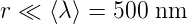
Die Streuung führt übrigens auch zu einer Polarisation.

(Siehe Haken, Wolf, Atom-und Quantenphysik [HW04, pp.
7-10])
Wenn ein Kristall immer weiter mit mechanischen Methoden zerkleinert wird, so scheint dies ein kontinuierlicher Prozess zu sein.
| Neuer Versuch zur Vorlesung: | |
| Kristall-Zerkleinerung | |
Warum muss man trotzdem annehmen, dass die Materie aus kleinsten Einheiten aufgebaut ist?
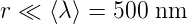
Die Streuung führt übrigens auch zu einer Polarisation.
Alle diese Experimente ergaben, dass die Anzahl der Teilchen aus der Molzahl der Chemiker berechnet werden konnte. Der Proportionalitätsfaktor heisst Avogadro-Zahl NA. Sie gibt an, wie viele Teilchen in einem Mol vorhanden sind. In Deutschland wird manchmal auch die Loschmidt-Zahl NL = NA verwendet, sie ist aber im Rest der Welt nicht gebräuchlich. Bei Kenntnis der Boltzmann-Konstante kB kann NA auf verschiedene Weise bestimmt werden:
__________________________________________________________________________
________________________________________________________________
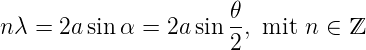 | (2.1) |
Aus dem Netzebenenabstand kann man das Volumen eines Atoms V A bestimmen. Die Avogadrozahl folgt dann aus
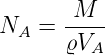 | (2.2) |
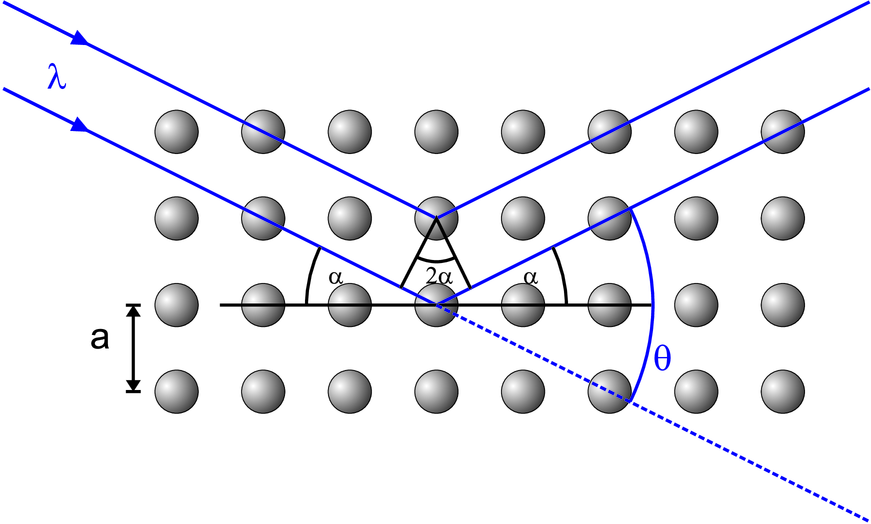
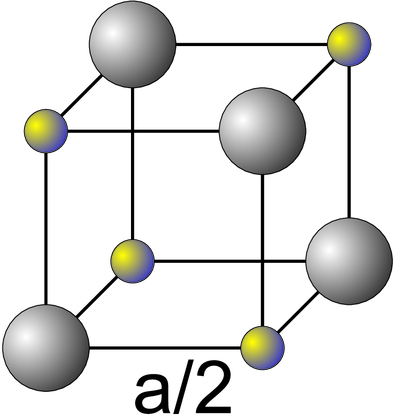
NaCl kristallisiert in einem kubischen Gitter mit dem Netzebenenabstand a, wobei sich in der Einheitszelle jeweils ein positives und ein negatives Ion befinden. Dies ist äquivalent zu dem Würfel in der Abbildung unten mit der halben Kantenlänge a∕2, wobei sich die positiven Na+-Ionen (klein) und die negativen Cl−-Ionen abwechseln.
__________________________________________________________________________
________________________________________________________________
Die Ionen an den Ecken sind Teil von 8 Würfeln, so dass in diesem Würfel mit dem Volumen (a∕2)3 netto ein Ion, also ein halbes NaCl liegt. Die Dichte der NaCl ist demnach
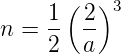 | (2.3) |
Mit V mol = NAV A = M∕ϱ bekommen wir aus (2.2) und aus (2.3)
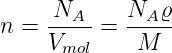 | (2.4) |
und damit
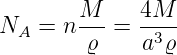 | (2.5) |
Mit den Daten ϱ = 1987 kgm−3 und M = 0.07455 kgmol sowie a = 629 pm bekommt man
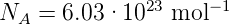
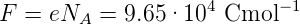 | (2.6) |
bestimmt werden. Damit ist auch die Avogadro-Zahl NA bestimmt.
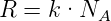 | (2.7) |
Die Gaskonstante R kann aus der Gleichung für ideale Gase abgeleitet werden, zum Beispiel aus pV -Diagrammen.
__________________________________________________________________________
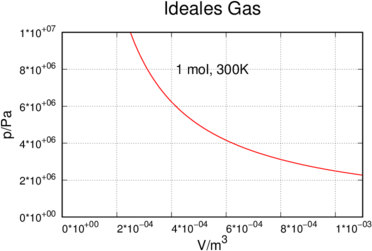
pV -Diagramm für ein ideales Gas
_____________________________________________________________________
Die Boltzmann-Konstante kann aus dem Sedimentationsgleichgewicht bestimmt werden (Jean-Babtiste Perrin[Per09], Nobelpreis 1926). Perrin erhielt für die Höhenverteilung der Teilchenzahl die folgende Gleichung:
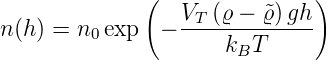 | (2.8) |
Hier ist V T das Volumen eines Teilchens, ϱ die Dichte
dieses Teilchens, 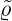 die Dichte der umgebenden Flüssigkeit,
g der Betrag des Feldvektors der Gravitation an der
Erdoberfläche (dem Ort des Experiments) und h die
Höhe über der Referenzstelle.
die Dichte der umgebenden Flüssigkeit,
g der Betrag des Feldvektors der Gravitation an der
Erdoberfläche (dem Ort des Experiments) und h die
Höhe über der Referenzstelle.
 Lizenzinformationen
Lizenzinformationen