©Ulm University 2012, Othmar Marti
[Nächste Seite] [Vorherige Seite]
[vorheriges Seitenende] [Seitenende] [Ebene nach oben] [PDF-Datei][Andere
Skripte]
35 Fluoreszenz-Korrelations-Spektroskopie
35.1 Lernziel
Die Fluoreszenz-Korrelations-Spektroskopie wurde in den frühen Siebzigerjahren
entwickelt, ist aber aufgrund technischer Entwicklungen, erst in den letzten Jahren
interessant geworden. In Verbindung mit einer konfokalen Optik kann Licht aus einem
sehr kleinen Volumenelement von nur 1μm3 (oder 1fl) zur Spektroskopie herangezogen
werden, und somit Proben in ebd. Volumen untersucht werden. Aus diesem Grund
wuchs die FCS in den letzten Jahren zu einer sehr leistungsfähigen Methode heran, um
dynamische Prozesse von gelösten Molekülen zu untersuchen. Die Vorteile liegen in der
hohen Auflösung, so dass eventuell sogar einzelne Moleküle betrachtet werden können,
in der geringen benötigten Probenmenge und der kurzen Aufnahmezeit von nur wenigen
Sekunden.
Das Funktionsprinzip eines Fluoreszenz-Korrelations-Spektrometers ist folgendes:
Durch sehr gute Fokussierung eines Lasers in einer Flüssigkeit und späteren
Strahlengang durch ein Pinhole wird ein sehr kleines Beobachtungsvolumen aus der
Flüssigkeit herausgegriffen. Fluoreszenz-Photonen aus diesem Volumen werden in
Abhängigkeit der Zeit gezählt. Nun analysiert man die Intensitätsschwankungen des
Fluoreszenzlichts. Diese hängen natürlich von den Fluktuationen der fluoreszierenden
Moleküle ab, welche durch Bewegung der Teilchen aufgrund von Diffusion (Brown’sche
Bewegung) oder Reaktionen der Moleküle in einen nichtfluoreszierenden Zustand (z.B.
Triplettzustand) verursacht werden. Aus diesem Grund kann man mit FCS z.B.
Diffusionskoeffizienten oder Ratenkonstanten für photophysikalische und chemische
Reaktionen bestimmen.
Wichtig für ein Fluoreszenz-Korrelations-Experiment ist die sogenannte
Autokorrelationsfunktion G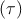 . Diese beschreibt die Selbstähnlichkeit des
Fluoreszenzsignals zu verschiedenen Zeiten t und t + τ und liefert damit Informationen
über die Zeitskalen der beteiligten Prozesse. Dazu werden die Fluktuationen
δF
. Diese beschreibt die Selbstähnlichkeit des
Fluoreszenzsignals zu verschiedenen Zeiten t und t + τ und liefert damit Informationen
über die Zeitskalen der beteiligten Prozesse. Dazu werden die Fluktuationen
δF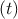 = F
= F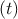 -
-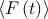 (Abweichung der momentanen Fluoreszenz vom Mittelwert)
eines bestimmten Zeitpunktes t mit den Fluktuationen des Zeitpunktes t + τ
multipliziert. Normiert ergibt sich dann folgende Form:
(Abweichung der momentanen Fluoreszenz vom Mittelwert)
eines bestimmten Zeitpunktes t mit den Fluktuationen des Zeitpunktes t + τ
multipliziert. Normiert ergibt sich dann folgende Form:
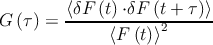 | (35.1) |
Der zeitliche Verlauf von G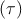 enthält nun Informationen
über die charakteristischen Zeiten der beteiligten dynamischen
Prozesse .
enthält nun Informationen
über die charakteristischen Zeiten der beteiligten dynamischen
Prozesse .
35.2 Lerninhalte
- Diffusion und Brownsche Bewegung
- Fluoreszenzfarbstoffe
- Optische Messung der Fluoreszenz
- Autokorrelationen und der Zusammenhang mit Diffusion und Chemische
Reaktion
35.3 Aufgaben
35.3.1 Erster Versuchstag:
- Bestimmung des Beobachtungsvolumens mit Rhodamin 6G
- Legen Sie ein Deckglas als Justierprobe auf und optimieren Sie den
konfokalen Aufbau mithilfe des Reflexes der Glas-Luft Grenzfläche des
Deckglases.
- Präparieren Sie eine „Sandwich-Probenkammer“ aus 2 Deckgläsern,
beschichten Sie diese mit BSA (Rinderserum-Albumin) und führen Sie
zunächst FCS-Messungen an einer 20nM Rh6G-Lösung in Wasser bei
geringer Laserleistung (ca. 50μW) durch.
- Bestimmen Sie aus diesen Messungen mit Hilfe des bekannten
Diffusionskoeffizienten für Rhodamin 6G die Geometrie des konfokalen
Volumens und die Konzentration der Rhodaminprobe.
- Wiederholen Sie die Messungen bei höherer Intensität (Laserleistung
zwischen 100μW und 500μW). Wie verändert sich die effektive
Teilchenzahl im konfokalen Volumen und die Korrelationszeit? Wie
lassen sich diese Veränderungen erklären?
- Bauen Sie statt des 50μm Pinholes nun ein Pinhole mit 30μm
Durchmesser ein und charakterisieren Sie für diese Geometrie Form und
Größe des konfokalen Volumens.
35.3.2 Zweiter Versuchstag:
- Bindung eines fluoreszenten Oligonukleotids an seinen Komplementärstrang
- Führen Sie
FCS-Messungen an einer Lösung aus Alexa555-fluoreszenzmarkierten,
kurzen DNA-Strängen (Oligonukleotiden) durch, die aus 8 Basen
(5’-GGTGAATG) bestehen. Bestimmen Sie den hydrodynamischen
Radius der Oligonukleotide.
- Untersuchen Sie nun
einige Proben, die zusätzlich verschiedene Konzentrationen (5nM bis
5μM) eines komplementären Oligonukleotids enthalten, welches durch
Kopplung an ein Streptavidin-Molekül eine wesentlich größere Masse
(geringere Beweglichkeit) hat.
- Tragen Sie die gemessenen Korrelationszeiten über der Konzentration
auf und ermitteln
Sie die Bindungskonstante (Dissoziations-Gleichgewichtskonstante).
Ermitteln Sie aus der Korrelationszeit bei Bindungssättigung den
hydrodynamischen Radius der gebundenen Spezies.
- Schätzen Sie aus der ermittelten Bindungskonstante die Ratenkonstante
für die Dissoziation (koff) der DNA-Stränge ab, indem Sie eine
diffusionskontrollierte Assoziation annehmen (kon ≈ 108M-1s-1).
Vergleichen Sie diese mit der Biotin-Streptavidin-Bindung!
35.4 Literatur
-
C. Röcker, G.U. Nienhaus
- Ausführliche Anleitung zum Versuch
-
R. Rieger, C. Röcker, G.U. Nienhaus
- „Fluctuation correlation spectroscopy for
the advanced physics laboratory“ Am. J. Phys. 73, 1129-1134 (2005)
-
A. Schenk
- „Fluorescence fluctuation spectroscopy -
Theoretical basis, experimental realization and applications to biomolecular
systems“Dissertation, Ulm 2003
-
E. Haustein, P. Schwille
- „Ultrasensitive investigations of biological systems by
fluorescence correlation spectroscopy“ Methods 29, 153 - 166 (2003)
-
R. Rigler, E.S. Elson (Eds.)
- „Fluorescence Correlation Spectroscopy, Theory
and Applications“ Springer, 2001, ISBN 3-540-67433-0
-
A. Einstein
- „Über die von der molekularkinetischen Theorie der Wärme geforderte
Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen“ Ann. Phys.
17, 549-460 (1905)
[Nächste Seite] [Vorherige Seite] [vorheriges Seitenende] [Seitenanfang] [Ebene nach
oben]
©Ulm University 2012, Othmar Marti
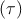 . Diese beschreibt die Selbstähnlichkeit des
Fluoreszenzsignals zu verschiedenen Zeiten t und t + τ und liefert damit Informationen
über die Zeitskalen der beteiligten Prozesse. Dazu werden die Fluktuationen
δF
. Diese beschreibt die Selbstähnlichkeit des
Fluoreszenzsignals zu verschiedenen Zeiten t und t + τ und liefert damit Informationen
über die Zeitskalen der beteiligten Prozesse. Dazu werden die Fluktuationen
δF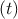 = F
= F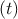 -
-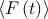 (Abweichung der momentanen Fluoreszenz vom Mittelwert)
eines bestimmten Zeitpunktes t mit den Fluktuationen des Zeitpunktes t + τ
multipliziert. Normiert ergibt sich dann folgende Form:
(Abweichung der momentanen Fluoreszenz vom Mittelwert)
eines bestimmten Zeitpunktes t mit den Fluktuationen des Zeitpunktes t + τ
multipliziert. Normiert ergibt sich dann folgende Form: