__________________________________________________________________________
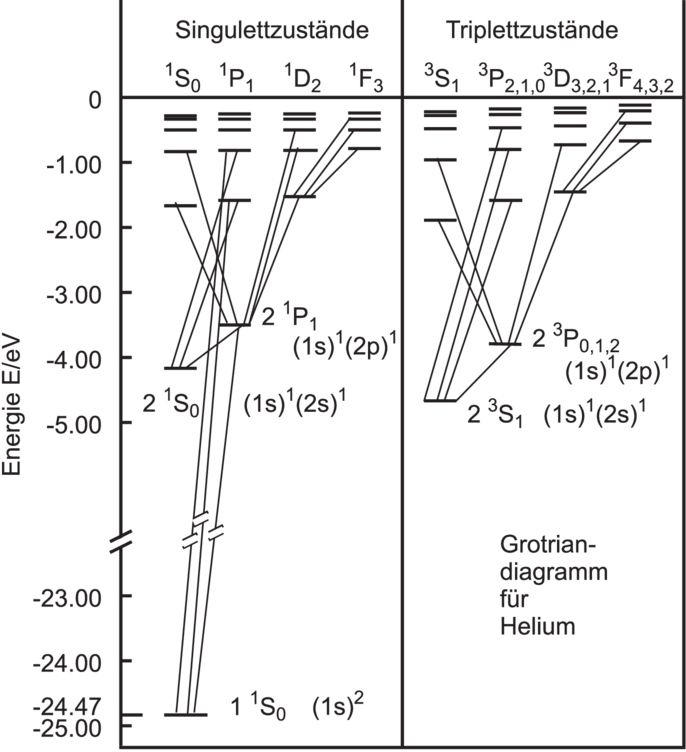
Termschema von Helium
_____________________________________________________________________

Elektronenzustände in Atomen mit mehreren Elektronen werden der Reihe nach von tiefen Energien zu hohen besetzt.
__________________________________________________________________________

Termschema von Helium
_____________________________________________________________________
Abbildung 6.8 zeigt das Grotrian-Diagramm oder Termschema von Helium. Es gibt zwei System, die keine Verbindung miteinander haben. Links ist das Singulettsystem und rechts das Triplettsystem. Sowohl der tiefste Zustand des Triplettsystems 23S 1-Zustand mit der Struktur (1s)1(2s)1 wie auch der zweittiefste Zustand im Singulettsystem 21S 0-Zustand mit der Struktur (1s)1(2s)1 sind metastabil. Metastabil bedeutet, dass die Lebensdauer τmetastabil » 10−8 s ist. 10−8 s ist eine übliche Lebensdauer für erlaubte Zustände. Metastabile Zustände werden über Dipol-verbotene Übergänge entleert.
Wenn ein Elektron aus dem Grundzustand in den angeregten Zustand wechselt, ändern sich die Quantenzahlen
___________________________________________________________________________
| vor der | 1.Elektron | n = 1 | ℓ = 0 | m = 0 | s = 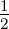 | sz = 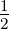 |
| Anregung | 2.Elektron | n = 1 | ℓ = 0 | m = 0 | s = 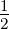 | sz = −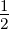 |
| nach der | 1. Elektron | n = 1 | ℓ = 0 | m = 0 | s = 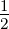 | sz = 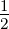 |
| Anregung | 2. Elektron | n > 1 | ℓ = 1 | m = −1…1 | s = 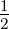 | sz = ±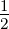 |
_____________________________________________________________________
Man bezeichnet He im Singulett-System als Parahelium, He im Triplettsystem wird als Orthohelium bezeichnet. Im Singulettsystem von Helium wird keine Feinstruktur beobachtet. Das bedeutet, dass die Spins der Elektronen antiparallel sein müssen.
Man bezeichnet mit grossen Buchstaben das gesamte System, mit kleinen Buchstaben die Zustände der einzelnen Elektronen. So ist der Gesamtspin
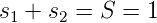
Das magnetische Moment des Gesamtspins μS hat drei Einstellmöglichkeiten:
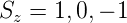 | (6.1) |
Wenn der Spin drei Einstellmöglichkeiten hat führt die Spin-Bahn-Kopplung zu einer dreifachen Feinstrukturaufspaltung.
Im Triplettzustand, beim Orthohelium, stehen die Spins parallel. Zwischen den entsprechenden Zuständen des Paraheliums und des Orthoheliums gibt es eine Energiedifferenz. Dies beruht auf der unterschiedlichen elektrostatischen Wechselwirkung bei parallel und antiparallel angeordneten Spins. So liegt der Zustand 21S 0 über dem Zustand 23S 1. Den Energieunterschied nennt man Symmetrie-Energie.
Im Helium muss man die Energie der Elektronen so schreiben
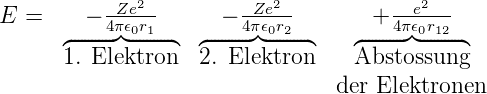 | (6.2) |
Damit ist die potentielle Energie nicht mehr kugelsymmetrisch. Die Wellenfunktion kann nicht mehr in einen Radial- und einen Winkelanteil separiert werden. Deshalb ist die Schrödingergleichung nicht geschlossen lösbar. Näherungsweise kann sie mit der Störungsrechnung gelöst werden. Als erste Näherung vernachlässigt man den Abstossungsterm zwischen den beiden Elektronen 1 und 2
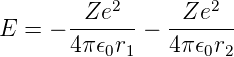 | (6.3) |
Dieses vereinfachte Problem ist lösbar. Die so berechneten Energien für die Ionisierung sind
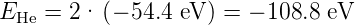 | (6.4) |
Experimentell hat man die folgenden Werte gemessen:
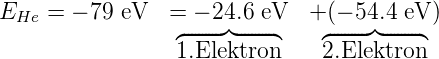 | (6.5) |
Die gesamte Ionisierungsenergie ist kleiner als die theoretische Vorhersage ohne gegenseitige Wechselwirkung der Elektronen. Die gegenseitige Abstossung verringert offensichtlich den Abstand zum Vakuumniveau. Das erste Elektron hat eine kleiner Ionisierungsenergie als das Elektron des Wasserstoffs. Die Ionisierungsenergie des zweiten Elektrons (wenn das erste schon weg ist) ist ziemlich genau das Doppelte des Wertes für den Wasserstoff. Den vierfachen Wert würde man auch aus der doppelt so grossen Kernladung erwarten.
Man könnte argumentieren, dass das äussere Elektron wegen der Abschirmung die Kernladung Z = 1 sieht, und nicht Z = 2. Dann wäre aber
Dies ist ein besserer Schätzwert, aber trotzdem immer noch falsch.
Da bei Helium zwar der Zustand 11S gibt, nicht aber den Zustand 13S bei dem zwei Elektronen im Grundzustand mit parallelem Spin vorhanden wären, folgerte Wolfgang Pauli
| Die Elektronenzustände eines Atoms können mit Elektronen nur so besetzt werden, dass nie zwei oder mehr Elektronen in allen Quantenzahlen übereinstimmen. |
Dieses ist das fundamentale Pauli-Prinzip. Die allgemein gültige mathematische Formulierung des Pauli-Prinzips lautet:
Bei Spin- -Teilchen ist Gesamtwellenfunktion -Teilchen ist Gesamtwellenfunktion
antisymmetrisch bei der Vertauschung zweier Variablen sein. |
Wenn wir zwei Teilchen haben, ist die mögliche Wellenfunktion
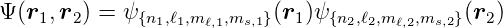 | (6.8) |
eine Wellenfunktion mit der Energie
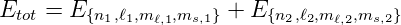 | (6.9) |
Die Wellenfunktion aus Gleichung (6.8) ist auch erlaubt, wenn
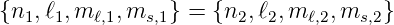
ist. Da mit der Wellenfunktion aus Gleichung (6.8) auch
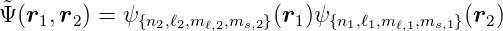
die zugrunde liegende Schrödingergleichung erfüllt, sind auch alle Linearkombinationen dieser beiden Wellenfunktionen Lösungen der Schrödingergleichung. Die Wellenfunktion
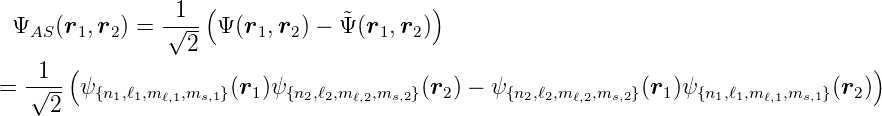 | (6.10) |
ist eine Lösung der Schrödingergleichung. Sie verschwindet aber identisch, wenn
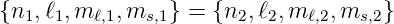
ist. Die Wellenfunktion ΨAS ist kompatibel mit dem
Pauli-Prinzip. Wann immer alle Indizes der beiden
Teilwellenfunktionen identisch sind, ist sie null. Die
Koordinaten 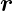 i können alle Variablen sein, sie müssen nicht
notwendigerweise Vektoren sein, es können auch zahlenwertige
Funktionen und insbesondere auch Spinfunktionen sein.
i können alle Variablen sein, sie müssen nicht
notwendigerweise Vektoren sein, es können auch zahlenwertige
Funktionen und insbesondere auch Spinfunktionen sein.
Wenn zwei Spins mit den möglichen Zuständen
mz,j = 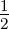 ℏ = ϕ↑(j) und mz,j = −
ℏ = ϕ↑(j) und mz,j = −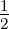 ℏ = ϕ↓(j) kombiniert
werden, ergeben sich
ℏ = ϕ↓(j) kombiniert
werden, ergeben sich
___________________________________________________________________________
| Singulettzustand | S = 0 | Φ = 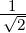 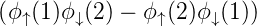 MS = 0 MS = 0 |
| Triplettzustand | S = 1 | Φ = 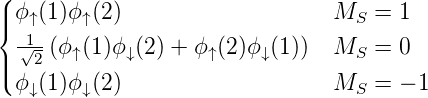 |
_____________________________________________________________________
Beim Wasserstoffatom wurde der Bahndrehimpuls 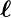 mit dem
Spin
mit dem
Spin 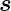 zum Gesamtdrehimpuls
zum Gesamtdrehimpuls 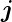 gekoppelt. Ähnliche
Mechanismen gibt es auch beim Gesamtbahndrehimpuls
gekoppelt. Ähnliche
Mechanismen gibt es auch beim Gesamtbahndrehimpuls 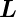 und dem Gesamtspin
und dem Gesamtspin 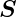 , die den Gesamtdrehimpuls
, die den Gesamtdrehimpuls 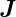 bilden.
Geschlossene Schalen, die Edelgasschalen, haben einen
Gesamtdrehimpuls null, so dass Atome allein durch die Spins
und die bahndrehimpulse der Valenzelektronen charakterisiert
werden.
bilden.
Geschlossene Schalen, die Edelgasschalen, haben einen
Gesamtdrehimpuls null, so dass Atome allein durch die Spins
und die bahndrehimpulse der Valenzelektronen charakterisiert
werden.
Wenn wir zum Beispiel zwei Bahndrehimpulse 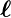 1 und
1 und
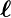 2 haben, können diese sich auf drei Arten zu einem
Gesamtbahndrehimpuls zusammensetzen:
2 haben, können diese sich auf drei Arten zu einem
Gesamtbahndrehimpuls zusammensetzen:
___________________________________________________________________________
| Anordnung | parallel | im Dreieck | antiparallel |
| Gesamtdrehimpuls | L = 2 | L = 1 | L = 0 |
| Bezeichnung | D-Term | P-Term | S-Term |
_____________________________________________________________________
In Atomen mit mehreren Elektronen gibt es die
Bahndrehimpulse 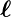 i und die Spins
i und die Spins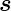 i. Es gibt nun drei
Wechselwirkungen,
i. Es gibt nun drei
Wechselwirkungen,
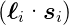
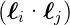
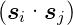
Wenn nun die Spin-Bahn-Kopplung 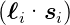 klein ist
gegen die Bahn-Bahn-Kopplung
klein ist
gegen die Bahn-Bahn-Kopplung 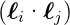 und gegen die
Spin-Spin-Kopplung
und gegen die
Spin-Spin-Kopplung 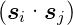 , dann addieren sich alle
Bahndrehimpulse und Spins getrennt bevor sie zum
Gesamtdrehimpuls zusammengesetzt werden.
, dann addieren sich alle
Bahndrehimpulse und Spins getrennt bevor sie zum
Gesamtdrehimpuls zusammengesetzt werden.
Aus dem Gesamtbahndrehimpuls 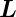 und dem Gesamtspin
und dem Gesamtspin 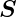 wird der Gesamtdrehimpuls gebildet
wird der Gesamtdrehimpuls gebildet
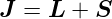 | (6.12) |
Bei der LS-Kopplung oder der Russel-Saunders-Kopplung
wird
|
Den Betrag des Gesamtbahndrehimpulses wird wie beim einzelnen Bahndrehimpuls berechnet
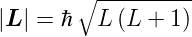 | (6.13) |
Wenn man alle möglichen Kombinationen zweier Vektoren
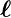 1 und
1 und 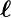 2 untersucht, also von parallel bis antiparallel,
dann sind die folgenden Bahndrehimpulsquantenzahlen
möglich
2 untersucht, also von parallel bis antiparallel,
dann sind die folgenden Bahndrehimpulsquantenzahlen
möglich
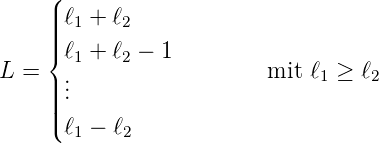 | (6.14) |
Man verwendet die folgenden Bezeichnungen
Für die optischen Übergänge gelten die folgenden Auswahlregeln
Für den Gesamtspin bei n Elektronen haben wir die Beziehungen
Für die Dipolstrahlung gilt die folgende Auswahlregel
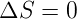 | (6.16) |
Die Auswahlregel aus Gleichung (6.16) besagt, dass Terme mit verschiedenem Gesamtspin nicht koppeln. Dies ist der Grund, warum zum Beispiel beim Helium das Singulett- und das Triplett-System nicht koppeln, da zwischen diesen Systemen mit unterschiedlichem Gesamtspin verboten sind.
Beim Gesamtdrehimpuls haben wir die Beziehungen
Für den Gesamtdrehimpuls 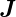 sind die folgenden Werte
möglich
sind die folgenden Werte
möglich
Insgesamt gibt es also 2S + 1 mögliche Kombinationen eines Gesamtbahndrehimpulses mit dem Gesamtspin zum Gesamtdrehimpuls
Zum Beispiel setzt sich bei He der Grundzustand wie folgt
zusammen: Es gibt zwei Elektronen mit der Hauptquantenzahl
n1 = n2 = 1. Diese haben jeweils den Bahndrehimpuls
ℓ1 = ℓ2 = 0 und die Spins s1 = 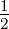 und s2 =
und s2 = 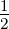 . Das bedeutet,
dass der Gesamtdrehimpuls L = 0 und der Gesamtspin S = 0.
Wenn ms1 = −ms2 ist, ist der Gesamtdrehimpuls J = 0. Dies
ist der beobachtete Singulettgrundzustand. Er wird mit 11S
0
bezeichnet.
. Das bedeutet,
dass der Gesamtdrehimpuls L = 0 und der Gesamtspin S = 0.
Wenn ms1 = −ms2 ist, ist der Gesamtdrehimpuls J = 0. Dies
ist der beobachtete Singulettgrundzustand. Er wird mit 11S
0
bezeichnet.
Andererseits ist bei L = 0, S = 1 für ms1 = ms2 der Gesamtdrehimpuls J = 1. Dieser Zustand mit dem Namen 13S 1 ist verboten (Wolfgang Pauli), da hier zwei Elektronen in allen Quantenzahlen übereinstimmen.
Wenn die beiden Elektronen unterschiedliche Hauptquantenzahlen haben, sind die möglichen Werte
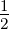
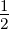
Dann ist entweder (L = 0, S = 0, J = 0, der Singulettzustand) oder (L = 0, S = 1, J = 1, der Triplettzustand). Beide Fälle mit den Namen 21S 0 und 23S 1 sind erlaubt und werden experimentell beobachtet.
| Zustände werden mit der folgenden Nomenklatur
n2S+1L
j bezeichnet. Dabei ist n die Hauptquantenzahl des höchsten angeregten Elektrons. |
_________________________________________________________________
| Anzahl Elektronen | 2 | 3 | 4 | 5 |
| Zustände | S = 0 | S = 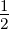 | S = 0 | S = 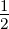 |
| Singulett | Dublett | Singulett | Dublett | |
| S = 1 | S = 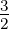 | S = 1 | S = 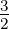 |
|
| Triplett | Quartett | Triplett | Quartett | |
| S = 2 | S = 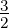 |
|||
| Quintett | Sextett |
_____________________________________________________________________
Tabelle 6.8.2.1 zeigt die möglichen Multiplettsysteme von Vielelektronenatomen.
Die Hundschen Regeln bei LS-Kopplung ergänzen das Pauli-Prinzip bei der Besetzung der Einelektronenzustände in einem Mehrelektronenatom.
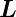 = 0 und den Gesamtspin
= 0 und den Gesamtspin 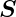 =
0.
=
0.
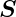 maximal ist.
maximal ist.
Dies bedeutet, dass Zustände mit der höchsten Multiplizität energetisch am tiefsten liegen. Die Gesamtwellenfunktion muss antiusymmetrisch sein.
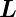
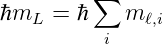
maximal ist. Dann ist die Drehimpulsquantenzahl
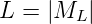
Zustände liegen bei gleicher Multiplizität 2S + 1 des Gesamtspins energetisch umso tiefer, je grösser L ist.
Diese vier Regeln, zusammen mit dem Pauli-Prinzip erlauben, die Grundzustände der Elektronen in allen Atomsorten zu bestimmen. Eine Übersicht über die erlaubten Zustände finden Sie in der Tabelle B im Anhang.
Bei schweren Atomen nimmt die Spin-Bahn-Kopplung mit der Kernladungszahl Z zu. Dann koppeln zuerst Spin und Bahndrehimpuls des Einzelelektrons
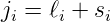 | (6.19) |
und erst dann wird der Gesamtdrehimpuls gebildet.
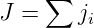 | (6.20) |
Wenn die jj-Kopplung dominiert, ist der Gesamtbahndrehimpuls
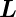 und der Gesamtspin
und der Gesamtspin 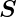 nicht mehr definiert. Der Betrag des
Gesamtdrehimpulses ist
nicht mehr definiert. Der Betrag des
Gesamtdrehimpulses ist
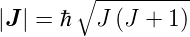 | (6.21) |
Die jj-Kopplung bewirkt das Auftreten von Interkombinationsfrequenzen. Sie tritt nur bei sehr schweren Atomen auf.
Die Auswahlregeln bei der jj-Kopplung sind
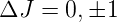 | (6.22) |
wobei der Übergang von J = 0 nach J = 0 verboten ist.
Das magnetische Moment bei LS-Kopplung ist
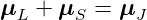 | (6.23) |
Wie schon beim Einzelelektron ist 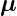 L antiparallel zum
Gesamtbahndrehimpuls
L antiparallel zum
Gesamtbahndrehimpuls 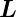 und
und 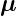 S antiparallel zum
Gesamtspin
S antiparallel zum
Gesamtspin 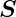 . Da für Bahndrehimpulse und Spins jedoch die
g-Faktoren unterschiedlich sind, ist
. Da für Bahndrehimpulse und Spins jedoch die
g-Faktoren unterschiedlich sind, ist 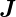 nicht antiparallel zu
nicht antiparallel zu 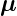 J.
Deshalb präzediert wie beim Einzelelektron das magnetische
Moment
J.
Deshalb präzediert wie beim Einzelelektron das magnetische
Moment 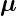 J um
J um 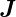 . Die Komponente
. Die Komponente 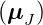 J von
J von 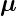 J, die
antiparallel zu
J, die
antiparallel zu 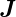 ist, ist das messbare magnetische Moment
des Gesamtspins.
ist, ist das messbare magnetische Moment
des Gesamtspins.
Der Betrag des magnetischen Moments des Gesamtspins ist
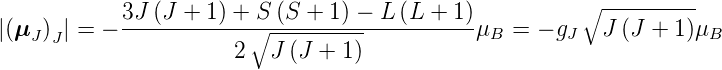 | (6.24) |
Hier ist der g-Faktor
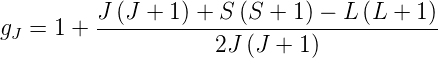 | (6.25) |
Schliesslich beträgt die z-Komponente des magnetischen Momentes
![[ ]
(μJ,z)J z = − mJ gJμB](ap-20151373x.png) | (6.26) |
mit der magnetischen Quantenzahl mJ = −J,−J + 1,…,J.
 Lizenzinformationen
Lizenzinformationen