Weiter: Wärmereservoire Oben: Wärmelehre Zurück: Wärmeleitung Skript: PDF-Datei Übungen: Blätter
| Dieser Stoff wurde am 11. 06. 2007 behandelt |
|
|
Materialien
Folien zur Vorlesung am 11. 06. 2007 PDF Übungsblatt 09 ausgegeben am 11. 06. 2007 |
Im ersten Hauptsatz haben wir die Konsequenzen der Energieerhaltung untersucht. Hier wollen wir nun die Eigenschaften kontinuierlich laufender Maschinen untersuchen.
| Jede kontinuierlich laufende Maschine muss periodisch oder zyklisch sein. Diese Prozesse heissen Kreisprozesse. |
| Der 2. Hauptsatz: Es gibt keine zyklische Maschine, die nur einem Wärmebad Energie entzieht und in mechanische Arbeit umwandelt. |
![\includegraphics[width=0.5\textwidth]{hauptsatz-zwei-011}](img1538.gif)
Reusenmaschine (analog zur Fischreuse)
|
Die Reusenklappen sollen so weich gelagert sein, dass ein Molekül, das von rechts kommt, sie aufstossen kann. Dadurch können zwar Moleküle von rechts nach links, nicht aber von links nach rechts gelangen. Der Druck (bei konstanter Temperatur) erhöht sich links, und der Kolben wird nach rechts bewegt, leistet also Arbeit. Wenn aber ein Molekül die Reusenklappen öffnen kann, bedeutet dies, dass Brownsche Bewegung (wegen der Temperatur der Reusenklappen) diese auch öffnen kann. Man könnte die Reusenklappen kühlen, dann hätte man aber zwei Wärmebäder.
![\includegraphics[width=0.5\textwidth]{hauptsatz-zwei-012}](img1539.gif)
Reusenmaschine mit Dämpfung
|
Hier gilt das gleiche: Die Dämpfung ist nur effektiv, wenn der Stossdämpfer
gekühlt wird ![]() . Dann hat man aber 2 Wärmereservoirs. Bei einer
elektrischen Dämpfung (Wirbelstrombremse) bringt das Widerstandsrauschen die
Klappen zum Schwingen. Dies funktioniert also auch nicht.
. Dann hat man aber 2 Wärmereservoirs. Bei einer
elektrischen Dämpfung (Wirbelstrombremse) bringt das Widerstandsrauschen die
Klappen zum Schwingen. Dies funktioniert also auch nicht.
![\includegraphics[width=0.5\textwidth]{hauptsatz-zwei-013}](img1541.gif)
Ratschenmaschine nach Feynman
|
Die Brownsche Bewegung dreht die Maschine. Die Klinke bewirkt, dass die Maschine sich nur in eine Richtung bewegen kann. Die Rätschenmaschine ist kein Perpetuum Mobile zweiter Art, da die Ratsche, analog zu oben, so leicht sein muss, dass sie wegen ihrer Brownschen Bewegung ohne Dämpfung hochspringen (elastisch) würde.
| Es ist kein Perpetuum Mobile 2. Art möglich. |
![\includegraphics[width=0.5\textwidth]{hauptsatz-zwei-014}](img1542.gif)
Perpetuum Mobile mit Wechselstrom-Elektromotor
|
Der verwendete Wechselstrommotor soll ein idealer Motor (ohne Innenwiderstand)
sein. Unabhängig von der Richtung und der Grösse der angelegten Spannung soll
er sich in die gleiche Richtung drehen. Hier nutzen wir die Rauschspannung am
Widerstand ![]() aus. Diese dreht den Motor: ein Perpetuum Mobile der 2. Art.
aus. Diese dreht den Motor: ein Perpetuum Mobile der 2. Art.
Auch hier funktioniert das nicht, da der Motor durch die Brownsche Bewegung des Ankers genauso wie der Widerstand eine Rauschspannungsquelle ist. Der Motor wirkt also als Generator. Um eine mechanische Arbeit zu leisten, müsste der Motor gekühlt werden.
![\includegraphics[width=0.5\textwidth]{hauptsatz-zwei-015}](img1543.gif)
![\includegraphics[width=0.3\textwidth]{hauptsatz-zwei-016}](img1544.gif)
Perpetuum Mobile
zweiter Art mit idealer Diode. Rechts ist die Kennlinie einer idealen Diode.
|
Eine ideale Diode ![]() hat in die eine Polarisationsrichtung den Widerstand null
und in die andere den Widerstand unendlich. Hier lädt also die Rauschspannung
über die Diode
hat in die eine Polarisationsrichtung den Widerstand null
und in die andere den Widerstand unendlich. Hier lädt also die Rauschspannung
über die Diode ![]() den Kondensator
den Kondensator ![]() auf. Wenn die Spannung gross genug ist,
wird
auf. Wenn die Spannung gross genug ist,
wird ![]() über den Schalter
über den Schalter ![]() durch den Motor
durch den Motor ![]() entladen. Dieser leistet
mechanische Arbeit. Bei dieser Anordnung ist das Zittern des Motors nicht
relevant.
entladen. Dieser leistet
mechanische Arbeit. Bei dieser Anordnung ist das Zittern des Motors nicht
relevant.
Die Anordnung ist trotzdem kein Perpetuum Mobile 2. Art, da, wie in der Festkörperphysik oder der Vorlesung Physikalische Elektronik und Messtechnik gezeigt wird, es keine ideale Diode gibt.
Durch Betrachtung von Wahrscheinlichkeiten kann der Zweite Hauptsatz auf statistische Gesetze zurückgeführt werden.
Dies steht eventuell im Gegensatz zu der Betrachtung, die die Entropie aus der Definition einer Adiabaten abgeleitet hat.
![\includegraphics[width=0.4\textwidth]{hauptsatz-zwei-001}](img1545.gif)
Nach dem Öffnen verteilen sich die Moleküle auf
beiden Kästen. Der Umkehrprozess ist nicht beobachtbar.
|
Wir betrachten drei Teilchen, nummeriert von 1 bis 3, die entweder links oder rechts sind. Jedes Teilchen kann also die Zustände links oder rechts einnehmen.
In der Regel wird das gesamte Volumen so in Kompartimente eingeteilt, dass in jedem Kompartiment nur keines oder ein Molekül ist.
Die räumliche Ausdehnung von Mikrozuständen ist klein gegen die des gesamten Systems. Sie muss jedoch gross gegen die charakteristische Strukturlänge der Teilchen sein. Bei Helium zum Beispiel werden die Atome bezüglich der Mikrozustände als Punkte angesehen.
Die Konsequenz dieser Aussagen ist, dass die Betrachtung nur gilt, wenn die
charakteristischen Längen
![]() sind.
sind.
Zwischen der atomaren Betrachtung und der makroskopischen Physik, also bei Längenskalen von Nanometern bis Mikrometern spricht man von der mesoskopischen Physik, einem aktuellen Forschungsgebiet.
| Ein System im Gleichgewicht befindet sich mit gleicher Wahrscheinlichkeit in jedem ihm zugänglichen Zustand. |
Die nicht unterscheidbaren Mikrozustände werden zu einem Makrozustand zusammengefasst. Sein statistisches Gewicht entspricht der Anzahl Mikrozustände.
Betrachtet man Makrozustände, sind die einzelnen Teilchen äquivalent oder ununterscheidbar.
|
Die drei Mikrozustände mit einem Teilchen links und zwei Teilchen rechts bilden einen Makrozustand.
|
Das Gewicht der einzelnen Makrozustände wird durch die Anzahl der Mikrozustände bestimmt.
Bei insgesamt ![]() Teilchen sind
Teilchen sind ![]() Teilchen im linken Kompartiment und
Teilchen im linken Kompartiment und ![]() Teilchen im rechten Kompartiment. Das Statistische Gewicht dieses Zustandes
ist
Teilchen im rechten Kompartiment. Das Statistische Gewicht dieses Zustandes
ist
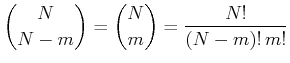 |
(4.398) |
Dies ist die Binominalverteilung (Siehe Bronstein, Taschenbuch der Mathematik [BSMM00, pp. 13]) .
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Für gross N geht die Binominalverteilung in die Gaussverteilung über.
Wir betrachten nochmals zwei Teilchen mit den Zuständen ![]() und
und
![]() . Die Teilchen sind mit den Wahrscheinlichkeiten
. Die Teilchen sind mit den Wahrscheinlichkeiten ![]() im
Zustand
im
Zustand ![]() und mit der Wahrscheinlichkeit
und mit der Wahrscheinlichkeit
![]() im
Zustand
im
Zustand ![]() .
.
|
Insgesamt gibt es ![]() Mikrozustände verteilt auf 4 Makrozustände.
Mikrozustände verteilt auf 4 Makrozustände.
Allgemein gibt es bei ![]() Teilchen mit
Teilchen mit ![]() Teilchen im Zustand
Teilchen im Zustand
![]() und
und ![]() Teilchen im Zustand
Teilchen im Zustand ![]()
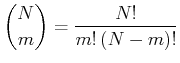 |
Zustände, jeweils mit dem statistischen Gewicht
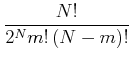 |
Die Gesamtzahl aller Mikrozustände ist ![]() .
.
Wenn man Zahlenwerte einsetzt, sieht man, dass extreme Makrozustände - alle Teilchen im gleichen Zustand - extrem selten sind.
![\includegraphics[width=0.7\textwidth]{hauptsatz-zwei-002}](img1559.gif)
Statistisches Gewicht, oder Wahrscheinlichkeit, für Makrozustände
mit
|
Um den Zustand eines Systems anzugeben bestimmt man zuerst seinen Mikrozustand.
Dabei sind die ![]() 's die zu den Ortskoordinaten
's die zu den Ortskoordinaten ![]() konjugierten Impulse.
Bei kartesischen Koordinaten ohne Magnetfeld und innere Freiheitsgrade gilt
konjugierten Impulse.
Bei kartesischen Koordinaten ohne Magnetfeld und innere Freiheitsgrade gilt
![]() . Mit Magnetfeld oder inneren Freiheitsgraden sind die
. Mit Magnetfeld oder inneren Freiheitsgraden sind die ![]() auf
eine kompliziertere Weise definiert.
auf
eine kompliziertere Weise definiert.
Der Vektor
beschreibt den Mikrozustand des Systems.
|
Ort
|
Die Position eines Teilchens mit dem Ort ![]() und dem Impuls
und dem Impuls ![]() kann, analog zu
den Fahrplänen aus der Vorlesung Grundlagen I im Phasenraum dargestellt werden.
kann, analog zu
den Fahrplänen aus der Vorlesung Grundlagen I im Phasenraum dargestellt werden.
![\includegraphics[width=0.7\textwidth]{hauptsatz-zwei-004}](img1577.gif)
Phasenraum eines Teilchens in einer eindimensionalen Welt.
|
Um Zustände definieren zu können, unterteilen wir den Phasenraum in Zellen mit
den Seiten ![]() und
und ![]() .
.
Das Phasenraumvolumen ist dann
mit der Einheit
![]() . In der
klassischen Physik (hier) ist
. In der
klassischen Physik (hier) ist ![]() eine variable Grösse, die man am Ende jeder
Rechnung gegen null gehen lässt. In der Quantenmechanik hat das
Phasenraumvolumen eines Teilchens in einer Dimension eine feste Grösse
eine variable Grösse, die man am Ende jeder
Rechnung gegen null gehen lässt. In der Quantenmechanik hat das
Phasenraumvolumen eines Teilchens in einer Dimension eine feste Grösse
Wir zählen nun die Phasenraumzellen ab. Die Koordinaten sagen dann, in welcher
Phasenraumzelle ein Teilchen sich gerade aufhält. Deshalb beschreibt ein ![]() - dimensionaler Vektor den momentanen Zustand eines
- dimensionaler Vektor den momentanen Zustand eines ![]() -Teilchen-Systems. Man
kann auch sagen, ein System aus
-Teilchen-Systems. Man
kann auch sagen, ein System aus ![]() Punktteilchen hat
Punktteilchen hat ![]() Freiheitsgrade.
Freiheitsgrade.
Bemerkung: Die statistische Mechanik und die statistische Interpretation der Quantenmechanik sind sich sehr ähnlich.
![\includegraphics[width=0.5\textwidth]{hauptsatz-zwei-005}](img1585.gif)
Die
Wahrscheinlichkeit, ein Teilchen in
|
Die Wahrscheinlichkeit, ein Teilchen in ![]() zu finden ist dann
zu finden ist dann
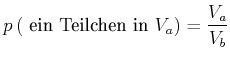 |
Für zwei Teilchen erhält man
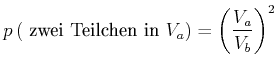 |
Für ![]() Teilchen im Volumen
Teilchen im Volumen ![]() bekommt man
bekommt man
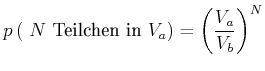 |
Wenn
![]() und
und
![]() Teilchen ist, beträgt die
Wahrscheinlichkeit dass alle Teilchen in
Teilchen ist, beträgt die
Wahrscheinlichkeit dass alle Teilchen in ![]() sind
sind
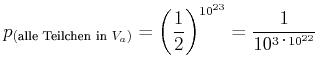 |
Bemerkung Die statistische Mechanik sagt nichts über die Geschwindigkeit aus, mit der Zustände erreicht werden.
| Ein Prozess heisst irreversibel, wenn sein Ausgangszustand versehen mit den statistischen Gewichten des Endzustandes unwahrscheinlicher ist als der Endzustand. |
| Eine Zustandsänderung heisst reversibel, wenn zwei Zustände über eine Kette von Zwischenzuständen so ineinander übergeführt werden, dass alle Zwischenzustände jeweils die maximale Wahrscheinlichkeit haben. |
| Dieser Stoff wurde am 14. 06. 2007 behandelt |
|
|
Materialien
Folien zur Vorlesung am 14. 06. 2007 PDF |
Wir zählen die Anzahl Zustände, die zwischen ![]() und
und
![]() liegen. In
vielen Fällen ist diese Energie die innere Energie
liegen. In
vielen Fällen ist diese Energie die innere Energie ![]() . Um auch die Fälle
mitzunehmen, bei denen die Gesamtenergie wesentlich durch andere Energien
bestimmt ist, verwenden wir hier den Buchstaben
. Um auch die Fälle
mitzunehmen, bei denen die Gesamtenergie wesentlich durch andere Energien
bestimmt ist, verwenden wir hier den Buchstaben ![]() . Solche Fälle sind, zum
Beispiel, die Thermodynamik in starken Lichtfeldern oder in der Nähe eines
schwarzen Lochs. Wir nennen diese Anzahl
. Solche Fälle sind, zum
Beispiel, die Thermodynamik in starken Lichtfeldern oder in der Nähe eines
schwarzen Lochs. Wir nennen diese Anzahl
Die Grösse ![]() muss so gewählt werden, dass sie klein gegen die Energie
selber ist, und dass sie gross gegen die internen Energieskalen (z.B. die
Abstände der quantenmechanischen Energieniveaux) ist. Aus der Anzahl der
Zustände definieren wir die Zustandsdichte
muss so gewählt werden, dass sie klein gegen die Energie
selber ist, und dass sie gross gegen die internen Energieskalen (z.B. die
Abstände der quantenmechanischen Energieniveaux) ist. Aus der Anzahl der
Zustände definieren wir die Zustandsdichte
![]() :
:
| (4.399) |
Wenn die Zustandsdichte bekannt ist, berechnen sich die Erwartungswerte der
Grössen ![]() wie
wie
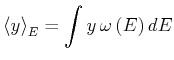 |
(4.400) |
Insbesondere ist der Erwartungswert der Energie
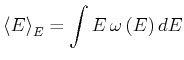 |
(4.401) |
Wie gross ist
![]() ? Wir nehmen an, dass das
System
? Wir nehmen an, dass das
System ![]() Freiheitsgrade hat. Für jeden Freiheitsgrad soll es
Freiheitsgrade hat. Für jeden Freiheitsgrad soll es
![]() Zustände geben. Dabei muss
Zustände geben. Dabei muss
![]() sein. Andererseits fällt auf jeden Freiheitsgrad die Energie
sein. Andererseits fällt auf jeden Freiheitsgrad die Energie
![]() . Die Gesamtzahl der Zustände
. Die Gesamtzahl der Zustände ![]() ist dann das
Produkt der Anzahl der einzelnen Zustände.
ist dann das
Produkt der Anzahl der einzelnen Zustände.
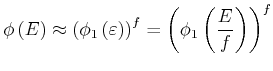 |
(4.402) |
Die Anzahl Zustände zwischen ![]() und
und
![]() , also in einer Kugelschale
einer
, also in einer Kugelschale
einer ![]() -dimensionalen Kugel der Dicke
-dimensionalen Kugel der Dicke ![]() berechnen5
berechnen5
Die Anzahl Zustände ![]() ändert sich langsam mit
ändert sich langsam mit
![]() , die Anzahl
der gesamten Zustände nimmt aber, da
, die Anzahl
der gesamten Zustände nimmt aber, da ![]() sehr gross ist, extrem schnell zu.
Dies gilt im allgemeinen für
sehr gross ist, extrem schnell zu.
Dies gilt im allgemeinen für
![]() und
und
![]() .
Logarithmieren wir Gleichung (4.125) und vernachlässigen konstante oder sich
nur langsam ändernde Terme (z.B.
.
Logarithmieren wir Gleichung (4.125) und vernachlässigen konstante oder sich
nur langsam ändernde Terme (z.B.
![]() oder
oder
![]() ), so erhalten wir
), so erhalten wir
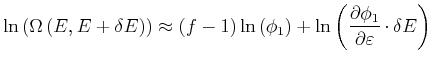 |
(4.404) |
Wenn ![]() die Grössenordnung
die Grössenordnung ![]() ist, ist auch
ist, ist auch
![]() . Da
. Da
![]() ist, ist der zweite Summand auch von der Grösse
ist, ist der zweite Summand auch von der Grösse ![]() .
.
Wir betrachten ![]() Moleküle eines monoatomaren Gases. Im allgemeinsten Fall
setzt sich die Gesamtenergie aus der kinetischen Energie der Teilchen und der
gegenseitigen Lageenergie (potentielle Energie) der Teilchen zusammen.
Moleküle eines monoatomaren Gases. Im allgemeinsten Fall
setzt sich die Gesamtenergie aus der kinetischen Energie der Teilchen und der
gegenseitigen Lageenergie (potentielle Energie) der Teilchen zusammen.
Die Anzahl Zustände zwischen ![]() und
und
![]() sind
sind
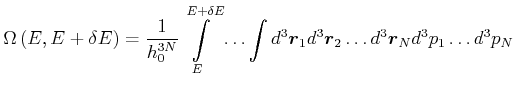 |
(4.405) |
Dies sind ![]() Integrale über den gesamten Phasenraum des Systems. Wir haben
die Abkürzungen
Integrale über den gesamten Phasenraum des Systems. Wir haben
die Abkürzungen
![]() und
und
![]() verwendet. Bei einem idealen Gas ohne
gegenseitige Wechselwirkung ist
verwendet. Bei einem idealen Gas ohne
gegenseitige Wechselwirkung ist ![]() . Deshalb ist das Integral über die
Raumkoordinaten einfach das Volumen zur
. Deshalb ist das Integral über die
Raumkoordinaten einfach das Volumen zur ![]() -ten Potenz.
-ten Potenz.
![$\displaystyle \int\limits_{E}^{E+\delta E}\ldots\int d^{3}\vec{r}_{1}\ldots d^{...
...\prod\limits_N \left[\int\limits_{E}^{E+\delta E} d^{3}\vec{r}_{i}\right]=V^{N}$](img1629.gif) |
(4.406) |
Die Integrale über die Impulse dürfen, bei einem idealen Gas, nur von der
gesamten kinetischen Energie ![]() abhängen.
abhängen.
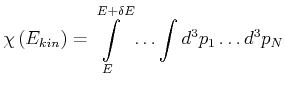 |
Damit erhalten wir
| (4.407) |
Aus der Mechanik ist bekannt, dass die gesamte kinetische Energie sich als Summe der kinetischen Energien der einzelnen Teilchen schreiben lässt:
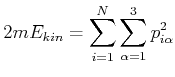 |
Dies ist die Bestimmungsgleichung einer ![]() -dimensionalen Kugel. Diese Kugel
hat den Radius
-dimensionalen Kugel. Diese Kugel
hat den Radius
![]() . Die Anzahl Zustände zwischen 0 und
. Die Anzahl Zustände zwischen 0 und ![]() hängt
dann vom Radius
hängt
dann vom Radius ![]() dieser Kugel ab und ist proportional zu
dieser Kugel ab und ist proportional zu
Da
![]() ist, gilt auch
ist, gilt auch
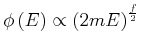 |
In der Kugelschale zwischen ![]() und
und
![]() liegen
liegen
Zustände. Hier haben wir verwendet, dass die Anzahl Freiheitsgrade ![]() ist.
Damit ist die Anzahl Zustände im Energiebereich zwischen
ist.
Damit ist die Anzahl Zustände im Energiebereich zwischen ![]() und
und
![]() durch
durch
| (4.408) |
Die Beziehung zwischen der Anzahl Zustände zwischen ![]() und
und
![]() vor
und nach einem Prozess erlauben, festzulegen, ob ein Prozess ein reversibler
Prozess ist. Sei
vor
und nach einem Prozess erlauben, festzulegen, ob ein Prozess ein reversibler
Prozess ist. Sei
![]() die Anzahl der Zustände im betrachteten
Energieintervall bevor wir den Prozess ausführen.
die Anzahl der Zustände im betrachteten
Energieintervall bevor wir den Prozess ausführen.
![]() sei
entsprechend die Anzahl der Zustände im betrachteten Energieintervall nach
Ausführung des Prozesses.
sei
entsprechend die Anzahl der Zustände im betrachteten Energieintervall nach
Ausführung des Prozesses.
|
Jedes thermodynamische System hat eine charakteristische Zeit ![]() , um ins
Gleichgewicht zu kommen. Diese charakteristische Zeit muss mit der
charakteristischen Zeit für ein Experiment,
, um ins
Gleichgewicht zu kommen. Diese charakteristische Zeit muss mit der
charakteristischen Zeit für ein Experiment, ![]() , verglichen werden.
, verglichen werden.
|
![\includegraphics[width=0.7\textwidth]{hauptsatz-zwei-006}](img1650.gif)
Skizze zweier thermodynamischer Systeme
|
Wir betrachten die beiden thermodynamischen Systeme ![]() und
und ![]() , die sich im
Kontakt binden sollen. Das Gesamtsystem
, die sich im
Kontakt binden sollen. Das Gesamtsystem
![]() sei thermisch isoliert.
Sei
sei thermisch isoliert.
Sei
![]() die Anzahl Zustände von
die Anzahl Zustände von ![]() zwischen
zwischen ![]() und
und
![]() und
und
![]() die Anzahl Zustände von
die Anzahl Zustände von ![]() zwischen
zwischen ![]() und
und
![]() .
.
Der Satz von der Energieerhaltung verlangt, dass
ist. Damit kann man die Energie ![]() von
von ![]() ausdrücken
ausdrücken
Wir bezeichnen mit
![]() die Anzahl
Zustände des Gesamtsystems
die Anzahl
Zustände des Gesamtsystems ![]() zwischen
zwischen ![]() und
und
![]() . Da die beiden
thermodynamischen Systeme
. Da die beiden
thermodynamischen Systeme ![]() und
und ![]() statistisch unabhängig sind, ist die
Anzahl der Zustände des Gesamtsystems das Produkt der Anzahl Zustände des
Systems
statistisch unabhängig sind, ist die
Anzahl der Zustände des Gesamtsystems das Produkt der Anzahl Zustände des
Systems ![]() , also
, also
![]() , und der Anzahl Zustände des Systems
, und der Anzahl Zustände des Systems
![]() , und
, und
![]() .
.
Die Wahrscheinlichkeit des Zustandes ![]() des Gesamtsystems ist
des Gesamtsystems ist
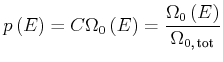 |
Dabei ist ![]() eine noch unbekannte Konstante und
eine noch unbekannte Konstante und
![]() die
Gesamtzahl aller möglicher Zustände summiert über alle Energien.
die
Gesamtzahl aller möglicher Zustände summiert über alle Energien.
Da die beiden thermodynamischen Systeme ![]() und
und ![]() statistisch unabhängig
sind, gilt
statistisch unabhängig
sind, gilt
| (4.409) |
Deshalb gilt für das Gesamtsystem ![]() die Wahrscheinlichkeit
die Wahrscheinlichkeit
| (4.410) |
![\includegraphics[width=0.6\textwidth]{hauptsatz-zwei-007}](img1666.gif)
Breite der Verteilungsfunktion
|
Für ![]() gilt:
gilt:
Begründung:
Daraus folgt für den Logarithmus von ![]()
Dabei existieren die folgenden Grenzwerte
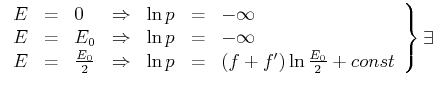 Maximum Maximum |
(4.411) |
Das Maximum von ![]() ist sehr viel schärfer als das Maximum von
ist sehr viel schärfer als das Maximum von ![]() .
.
Wie gross ist ![]() ? Diese Grösse kann über die Ableitung berechnet
werden.
? Diese Grösse kann über die Ableitung berechnet
werden.
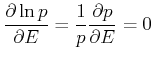 |
(4.412) |
Es gilt aber
| (4.413) |
Damit und mit
![]() erhalten wir
erhalten wir
| 0 | 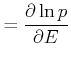 |
|
![$\displaystyle =\frac{\partial }{\partial E}\left[ \ln C+\ln \Omega \left( E\right) +\ln \Omega'\left( E'\right) \right]$](img1677.gif) |
||
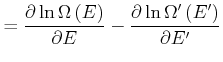 |
(4.414) |
Wir setzen
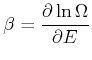 |
und erhalten im Gleichgewicht
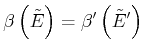 |
(4.415) |
mit
![]() .
.
Dieses ![]() ist eine Funktion von
ist eine Funktion von ![]() und hat als Einheit
und hat als Einheit
![]() . Andererseits wissen wir, dass auch die
Temperatur eine Funktion der Energie, nämlich der inneren Energie
. Andererseits wissen wir, dass auch die
Temperatur eine Funktion der Energie, nämlich der inneren Energie ![]() ist.
ist.
Wir definieren:
|
Dabei ist ![]() die Boltzmannkonstante und
die Boltzmannkonstante und ![]() die Temperatur.
die Temperatur.
Mit der (zuerst rein formalen) Definition der Entropie
| (4.417) |
bekommt man
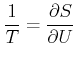 |
(4.419) |
![]() heisst Entropie. Ihre Einheit ist
heisst Entropie. Ihre Einheit ist
![]() .
.
|
ist die statistische Definition der Entropie |
In unserer Herleitung hängt die Anzahl der Zustände ![]() und die Entropie
und die Entropie ![]() immer noch von der konstanten
Breite des Energieintervalls
immer noch von der konstanten
Breite des Energieintervalls ![]() ab. Gleichung Gleichung (4.140) zeigt, dass
ab. Gleichung Gleichung (4.140) zeigt, dass ![]() unabhängig von
unabhängig von ![]() ist. Nehmen wir an, dass das Energieintervall von
ist. Nehmen wir an, dass das Energieintervall von ![]() auf
auf
![]() wechselt. Da die Zustandsdichten
gleich sind(
wechselt. Da die Zustandsdichten
gleich sind(
![]() ), gilt auch
), gilt auch
![]() und damit
und damit
![]() . Nun hat aber
. Nun hat aber ![]() die Grössenordnung
die Grössenordnung
![]() und
und
![]() liegt irgend wo bei einem Wert kleiner
liegt irgend wo bei einem Wert kleiner ![]() , so dass in
sehr guter Näherung gilt:
, so dass in
sehr guter Näherung gilt: ![]() . Damit ist auch die Entropie unabhängig von der Wahl von
. Damit ist auch die Entropie unabhängig von der Wahl von ![]() .
.
Der wahrscheinlichste Zustand unserer beiden thermodynamischen Systeme im Kontakt ist gegeben durch
| (4.420) |
| (4.421) |
Aus der statistischen Physik kann man ableiten:
|
Im Gleichgewicht zweier thermodynamischer Systeme sind
ihre Temperaturen gleich und die gesamte Entropie |
| Dieser Stoff wurde am 18. 06. 2007 behandelt |
|
|
Materialien
Folien zur Vorlesung am 18. 06. 2007 PDF Übungsblatt 10 ausgegeben am 22. 06. 2007 Lösungsblatt 10 ausgegeben am 22. 06. 2007 |
![\includegraphics[width=0.7\textwidth]{hauptsatz-zwei-008}](img1702.gif)
Überströmversuch
|
Beim Überströmversuch betrachtet man zwei Zustände, in denen ein System von ![]() Teilchen sich befinden kann.
Teilchen sich befinden kann.
|
Wenn das Gas also aus dem Zustand alles links in den gleichverteilten Zustand wechselt, ändert sich die Entropie um
Wenn ![]() Teilchen aus
Teilchen aus ![]() in
in ![]() strömen, nimmt die Entropie um
strömen, nimmt die Entropie um
![]() zu.
Andererseits müsste die Entropie um den gleichen Wert abnehmen, wenn alle
Teilchen aus dem gleichverteilten Zustand nach
zu.
Andererseits müsste die Entropie um den gleichen Wert abnehmen, wenn alle
Teilchen aus dem gleichverteilten Zustand nach ![]() strömen sollten.
strömen sollten.
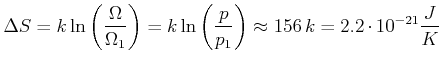 |
zugenommen.
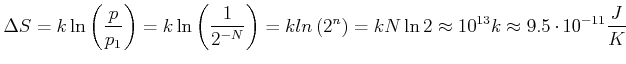 |
Wir wissen, dass die Beziehungen
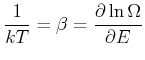 |
|
| (4.422) |
![$\displaystyle \frac{\partial \ln \Omega(E)}{\partial E} = \frac{\partial \left[f\ln
E\right]}{\partial E} = \frac{f}{E}$](img1722.gif) |
Weiter gilt, dass für alle ![]() auch
auch ![]() ist.
ist.
Aus
Dieses Resultat gilt, wenn |
Wenn ![]() eine obere Grenze hat dann gibt es Energien für die
eine obere Grenze hat dann gibt es Energien für die
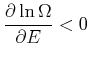 |
(4.424) |
Aus
![]() folgt
folgt
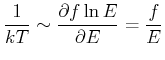 |
und weiter, dass
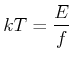 |
(4.425) |
Wenn kein Gleichgewicht herrscht, fliesst die (infinitesimale) Wärme
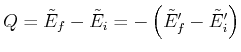 zwischen den beiden Wärmereservoiren. Die Entropie nimmt dann zu mit
zwischen den beiden Wärmereservoiren. Die Entropie nimmt dann zu mit
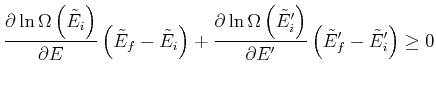 |
(4.426) |
also Wärme wird vom System mit den höheren ![]() (kleinerem
(kleinerem ![]() ) absorbiert
und von niederen
) absorbiert
und von niederen ![]() (höherem
(höherem ![]() ) abgegeben.
) abgegeben.
Othmar Marti