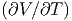 p,
p,
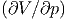 T und
T und 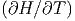 p berechnet werden. Diese Grössen
können gemessen werden:
p berechnet werden. Diese Grössen
können gemessen werden:

(Siehe Handbook of Chemistry and Physics [WA80, pp. D-120])
Die folgenden Funktionen werden betrachtet:
Aus den folgenden Tabellen können die ersten Ableitungen
von p, V , T, U, S, H, F und G als Funktion von 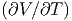 p,
p,
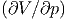 T und
T und 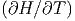 p berechnet werden. Diese Grössen
können gemessen werden:
p berechnet werden. Diese Grössen
können gemessen werden:
| α | = 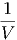 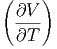 p p | isobare Volumenkompressibilität | (K.1) | |
| κ | = -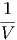 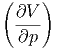 T T | isotherme Kompressibilität | (K.2) | |
| νcp,mol | = 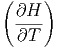 p p | molare Wärmekapazität bei konstantem Druck | (K.3) |
Beispiel:
Wir wollen 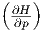 S als Funktion von T, p und V berechnen.
S als Funktion von T, p und V berechnen.
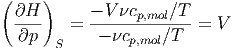 |
Wir wollen 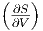 T als Funktion von T, p und V berechnen.
T als Funktion von T, p und V berechnen.
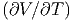 p.
p.
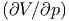 T .
T .
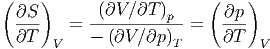 |
| Konstanten | ||
| Differenzial | T | p |
| T | 0 | 1 |
| p | -1 | 0 |
| V | -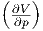 T T | 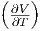 p p |
| S | 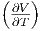 p p | 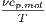 |
| U | T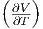 p + p p + p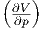 T T | νcp,mol - p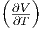 p p |
| H | -V + T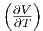 p p | νcp,mol |
| F | p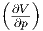 T T | -S - p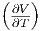 p p |
| G | -V | -S |
| Konstante | |
| Differenzial | V |
| T | 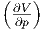 T T |
| p | -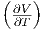 p p |
| V | 0 |
| S | 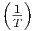 ![[ ( ) ( )2]
νcp,mol ∂∂Vp- T + T ∂∂VT- p](td-20152415x.png) |
| U | νcp,mol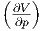 T + T T + T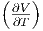 p2 p2 |
| H | νcp,mol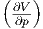 T + T T + T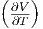 p2 - V p2 - V 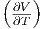 |
| F | -S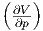 T T |
| G | -V 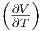 p - S p - S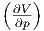 T T |
| Konstante | |
| Differenzial | S |
| T | -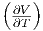 p p |
| p | -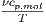 |
| V | 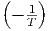 ![[ ( ) ( ) ]
νc ∂V- + T ∂V-2
p,mol ∂p T ∂T p](td-20152427x.png) |
| S | 0 |
| U | 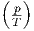 ![[ ( ) ( )2]
νcp,mol ∂∂Vp- + T ∂∂VT-
T p](td-20152429x.png) |
| H | -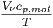 |
| F | 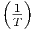 ![[ ( ) ( ) ( ) ]
p c ∂V- + pT ∂V-2 + T S ∂V-
ν p,mol ∂p T ∂T p ∂T p](td-20152432x.png) |
| G | 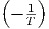 ![[ ( ) ]
νc V - T S ∂V-
p,mol ∂T p](td-20152434x.png) |
| Konstante | |
| Differenzial | U |
| T | -T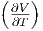 p - p p - p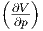 T T |
| p | -νcp,mol + p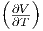 p p |
| V | -νcp,mol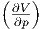 T - T T - T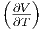 p2 p2 |
| S | 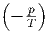 ![[ ( ∂V-) ( ∂V-)2]
νcp,mol ∂p T + T ∂T p](td-20152441x.png) |
| U | 0 |
| H | -V ![[ ( ) ]
νc - p ∂V-
p,mol ∂T p](td-20152442x.png) - p - p![[ ( ) ( ) ]
νc ∂V-- + T ∂V--2
p,mol ∂p T ∂T p](td-20152443x.png) |
| F | p![[ ( ) ( ) ]
νc ∂V- + T ∂V- 2
p,mol ∂p T ∂T p](td-20152444x.png) + S + S![[ ( ) ( ) ]
T ∂V- + p ∂V-
∂T p ∂p T](td-20152445x.png) |
| G | -V ![[ ( ) ]
νc - p ∂V-
p,mol ∂T p](td-20152446x.png) + S + S![[ ( ) ( ) ]
T ∂V- + p ∂V-
∂T p ∂p T](td-20152447x.png) |
| Konstante | |
| Differenzial | H |
| T | V - T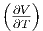 p p |
| p | -νcp,mol |
| V | -νcp,mol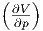 T - T T - T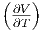 p2 + V p2 + V 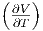 p p |
| S | 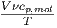 |
| U | V ![[ ( ∂V) [ ( ∂V) ( ∂V)2]]
νcp,mol - p ∂T-p + p νcp,mol ∂T-T + T ∂T-p](td-20152453x.png) |
| H | 0 |
| F | -![[ ]
(∂V-)
S + p ∂T p](td-20152454x.png) × ×![[ ]
(∂V) (∂V-)
V - T ∂T p - pνcp,mol ∂p T](td-20152455x.png) |
| G | -V νcp,mol - V S + TS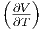 p p |
| Konstanten | |
| Differenzial | F |
| T | -p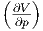 T T |
| p | S + p -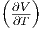 p p |
| V | S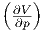 T T |
| S | 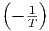 ![[ ( ) ( )2 ( ) ]
pνcp,mol ∂∂Vp- + pT ∂∂VT- + TS ∂∂VT-
T p p](td-20152461x.png) |
| U | -p![[ ( ) ( )2]
νcp,mol ∂∂Vp- + T ∂∂VT-
T p](td-20152462x.png) - S - S![[ ( ) ( ) ]
T ∂∂VT- + p ∂∂Vp-
p T](td-20152463x.png) |
| H | ![[ ( ) ]
S + p ∂∂VT-
p](td-20152464x.png) × ×![[ ( ) ( ) ]
V - T ∂∂VT- - pνcp,mol ∂∂Vp-
p T](td-20152465x.png) |
| F | 0 |
| G | S![[ ( ) ]
V + p ∂V-
∂p T](td-20152466x.png) + pV + pV 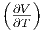 p p |
| Konstanten | |
| Differenzial | G |
| T | V |
| p | S |
| V | V 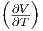 p + S p + S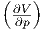 T T |
| S | 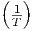 ![[ ( ) ]
νcp,molV - TS ∂V-
∂T p](td-20152471x.png) |
| U | V ![[ ( ) ]
νcp,mol - p ∂V-
∂T p](td-20152472x.png) - S - S![[ ( ) ( ) ]
T ∂V- + p ∂V-
∂T p ∂p T](td-20152473x.png) |
| H | V νcp,mol + V S - TS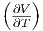 p p |
| F | -S![[ ( ∂V-) ]
V + p ∂p T](td-20152475x.png) + pV + pV 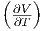 p p |
| G | 0 |
Abbildungsverzeichnis
Tabellenverzeichnis
 Lizenzinformationen
Lizenzinformationen