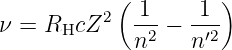
Licht mit hoher Energie wird nach Wilhelm Conrad Röntgen in Deutschland Röntgenstrahlen benannt, in anderen Sprachen heissen die Strahlen nach Röntgen „X-Strahlen“. Eine Abschätzung der Frequenz erlaubt die Serienformel nach Rydberg und Ritz
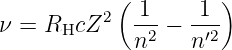 | (6.1) |
wobei RH = 10 970 955.31 m−1 die Rydbergkonstante ist. Bei Z = 20 ist die Frequenz und damit die Energie über Z2 = 400 mal grösser.
__________________________________________________________________________
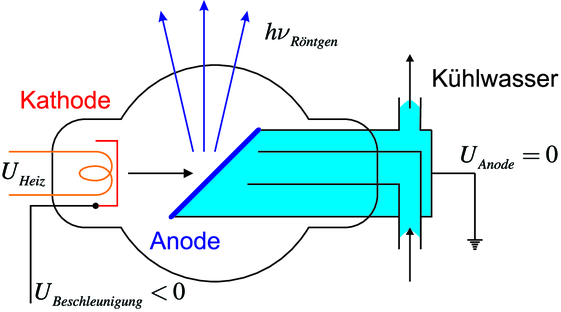
Skizze einer Röntgenröhre. Die Anode der Röntgenröhre muss mit Wasser gekühlt werden. Deshalb liegt sie auf Erde. Die indirekt geheizte Kathode liegt auf der negativen Beschleunigungsspannung. Das Material der Anode bestimmt das Spektrum der Röntgenstrahlung hνRöntgen.
_____________________________________________________________________
| Versuch zur Vorlesung: | |
| Röntgenfluoreszenz (Versuchskarte AT-24) | |
| Versuch zur Vorlesung: | |
| Absorption von Röntgenstrahlen: Qualitativ (Versuchskarte AT-40) | |
Röntgenstrahlen werden üblicherweise mit Röntgenröhren (siehe Abbildung 6.10) oder in Ausnahmefällen mit hochenergetischen Lasern hergestellt. Durch Frequenzvervielfachung [Sar+91] um einen Faktor 100 oder mehr wird langwelliges Röntgenlicht mit Wellenlängen von 5 nm bis 10 nm erzeugt.
__________________________________________________________________________
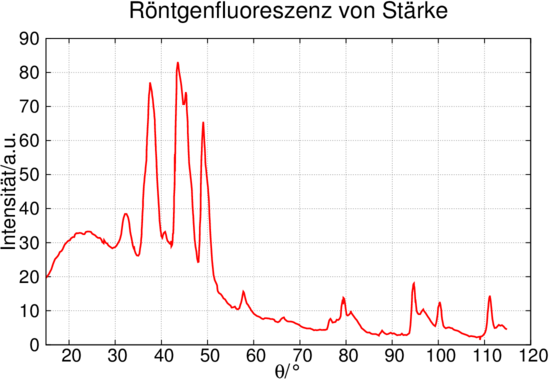
Röntgenfluoreszenz einer Stärkeprobe (adaptiert von [Gun57]).
_____________________________________________________________________
Röntgenfluoreszenz wird die gemischte Emission spezifischer und unspezifischer Röntgenstrahlung aus einer Probe bei deren Bestrahlung mit höherenergetischer Röntgenstrahlung genannt. Abbildung 6.10 zeigt, wie diese Röntgenfluoreszenz zur Identifikation von Elementen in einer Stärkeprobe verwendet werden kann. Die Details finden Sie in der Arbeit von Gunn [Gun57].
__________________________________________________________________________
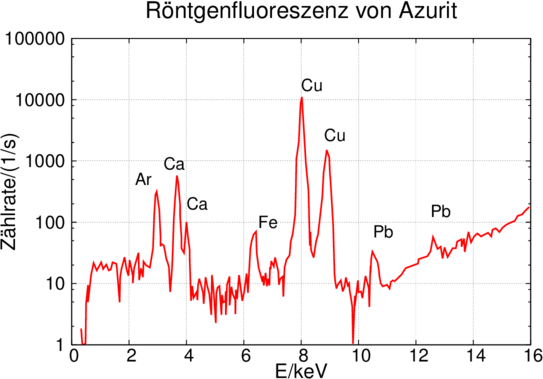
Röntgenfluoreszenz von Azurit oder Kupferlasur, einem Bestandteil eines Pigmentes in einem mittelalterlichen Manuskript aus der Bibliothek der Universität Ghent (adaptiert von [Weh+99]).
_____________________________________________________________________
Abbildung 6.10 zeigt ein weiteres Fluoreszenzspektrum. Es wurde von Wehling und Mitarbeitern [Weh+99] zur Untersuchung von Pigmenten mitelalterlicher Manuskripte gemessen.
| Versuch zur Vorlesung: | |
| Drehbares Kreuzgitter: Optisches Analogon zur Debye-Scherrer-Interferenz (Versuchskarte O-133) | |
_______________________________________________

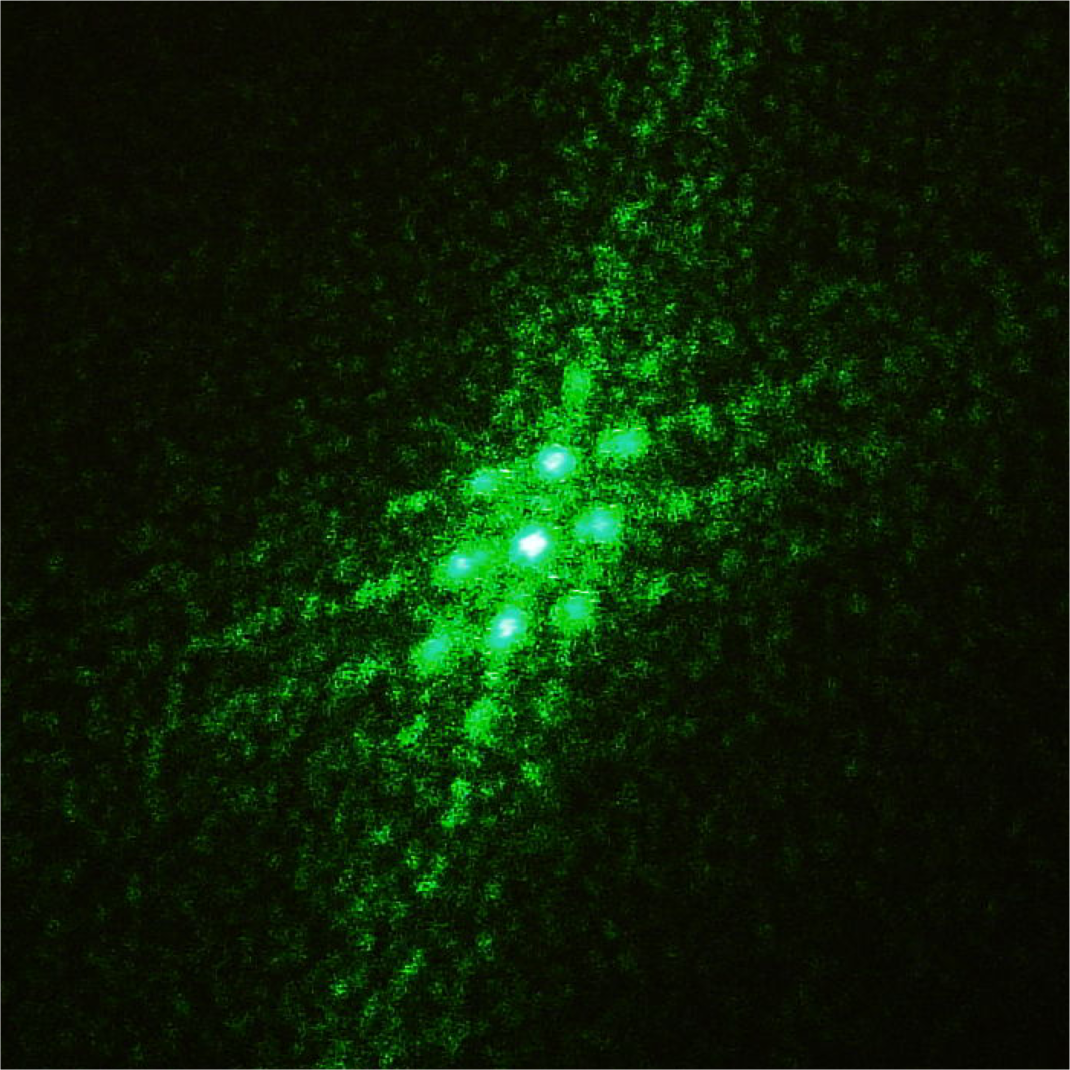
Optisches Analogon zur Röntgenbeugung. Links ist das Beugungsgitter, ein textiles Gewebe, gezeigt, rechts das dazugehörige Beugungsmuster.
_____________________________________________________________________
Abbildung 6.10.1 zeigt das beugende Gitter und dazu rechts das resultierende Beugungsmuster. Prinzipiell funktioniert die Röntgenbeugung analog zu diesem Experiment. Abbildung 6.10.1 zeigt das Beugungsmuster aus Abbildung 6.10.1 rotationsgemittelt um den Mittelpunkt des Beugungsmusters. Wenn viele identische Beugungsobjekte wie das textile Gewebe aus Abbildung 6.10.1 mit zufälliger Orientierung gleichzeitig untersucht werden, so erwartet man ein Beugungsbild nach Abbildung 6.10.1. Bei Kristallen ist dies die Pulvermethode nach Debye-Scherrer.
__________________________________________________________________________

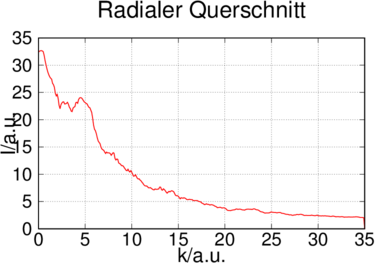
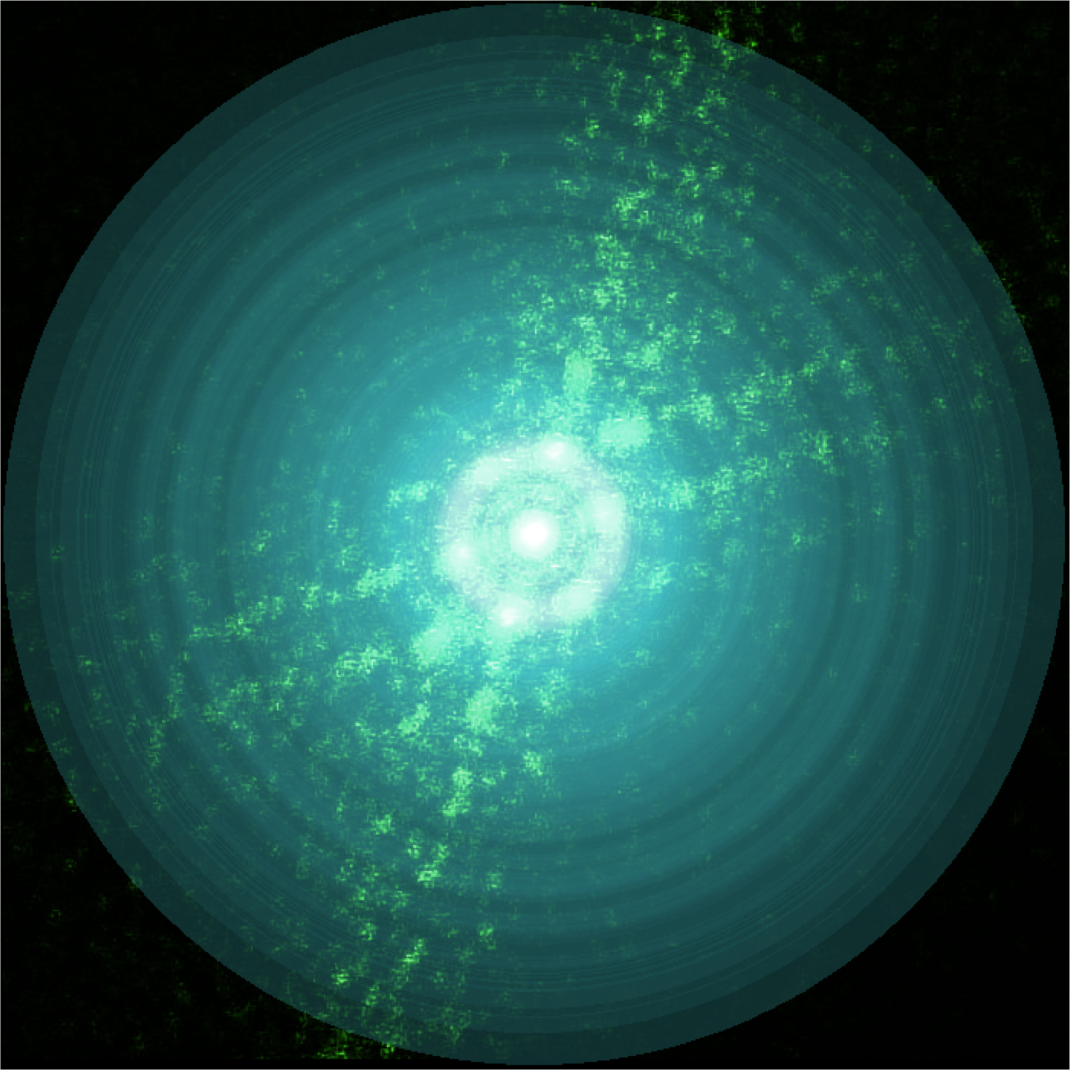
Analogon des Beugungsmusters nach Debye-Scherrer. Links ist das über alle Winkel ausgeschmierte Beugungsmuster aus Abbildung 6.10.1 gezeigt, in der Mitte das Profil des Querschnitts und rechts die logarithmisch skalierte Version des linken Bildes mit der Überlagerung des Beugungsmusters aus Abbildung 6.10.1.
_____________________________________________________________________
Die rechte Seite von Abbildung 6.10.1 zeigt schliesslich eine Überlagerung des Einzelbeugungsmusters mit dem rotationsgemittelten Muster. Klar ist die Übereinstimmung der hellen Ringe mit Beugungspunkten zu erkennen.
| Versuch zur Vorlesung: | |
| Röntgenstrahlung: Bremsstrahlung und charakteristische Linien (Versuchskarte AT-37) | |
Wenn Materie mit Röntgenlicht beleuchtet wird, entsteht ein Kontinuum und charakteristische Linien. Das kontinuierliche Spektrum heisst Bremsspektrum.
__________________________________________________________________________
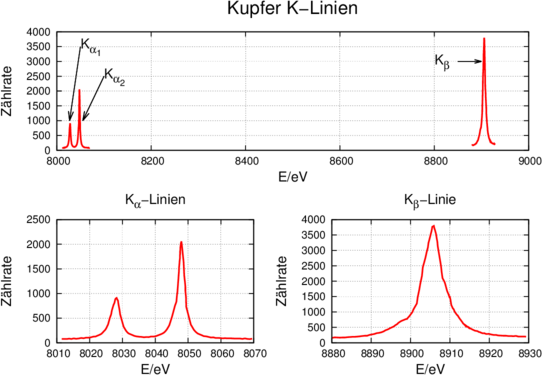
Kupfer-K-Linien (adaptiert aus [Deu+95]).
_____________________________________________________________________
Abbildung 6.10.2 zeigt am Beispiel der Cu-Kα1,2- und der Cu-Kβ-Linien, wie ein Röntgenspektrum aussehen kann. Die maximal mögliche Energie der Röntgenquanten ist durch die Differenzspannung zwischen Anode und Kathode, der Beschleunigungsspannung UB gegeben.
 | (6.2) |
__________________________________________________________________________
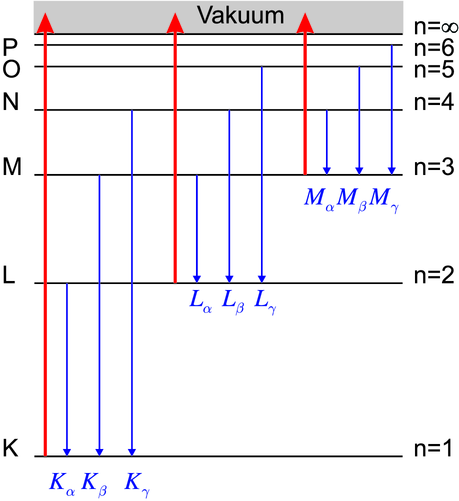
Bezeichnung der Übergänge zwischen den inneren Schalen
_____________________________________________________________________
Abbildung 6.10.2 zeigt schematisch die inneren Elektronenniveaus. Die roten Linien stellen die Ionisierung ins Vakuum dar. Wenn zum Beispiel ein Elektron von der L-Schale in die K-Schale relaxiert, nennt man die emittierte Röntgenlinie eine Kα-Linie. Die durch die Hauptquantenzahl n bezeichneten Niveaus werden durch die Spin-Spin-Kopplung und die Spin-Bahn-Kopplung aufgespalten.
___________________________________________________________________________
| Schale | n | ℓ | j | Bezeichnung |
| K | 1 | 0 | 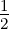 | 12S 1∕2 |
| LI | 2 | 0 | 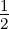 | 22S 1∕2 |
| LII | 2 | 1 | 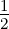 | 22P 1∕2 |
| LIII | 2 | 1 | 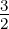 | 22P 3∕2 |
| MI | 3 | 0 | 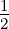 | 32S 1∕2 |
| MII | 3 | 1 | 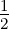 | 32P 1∕2 |
| MII | 3 | 1 | 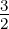 | 32P 3∕2 |
| MIV | 3 | 2 | 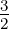 | 32D 3∕2 |
| MV | 3 | 2 | 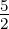 | 32D 5∕2 |
_____________________________________________________________________
Tabelle 6.10.2 gibt eine Auflistung der Bezeichnungen. Diese folgen der Konvention n2S+1L j (Siehe auch Abschnitt 6.8.2.1).
Abbildung 6.10.2 die radiale Elektronendichteverteilung von Wasserstoff und von einfach positiv geladenen Ionen. Je grösser die Kernladung ist, desto näher ist die K-Schale beim Kern.
__________________________________________________________________________
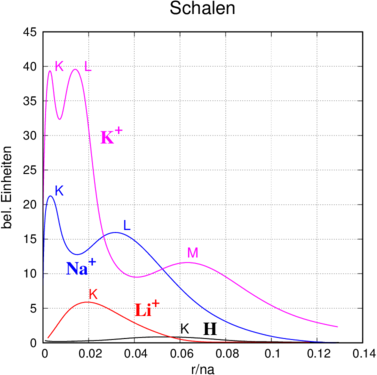
Schalenaufbau von H, Li+, Na+ und K+ nach [HW04, p. 351].
_____________________________________________________________________
Schliesslich zeigt Abbildung 6.10.2 die Ionisationszustände von Atomen aus dem Periodensystem. Mit Periodensystem wird die auf der Elektronenkonfiguration beruhende Anordnung der Elemente genannt.
__________________________________________________________________________
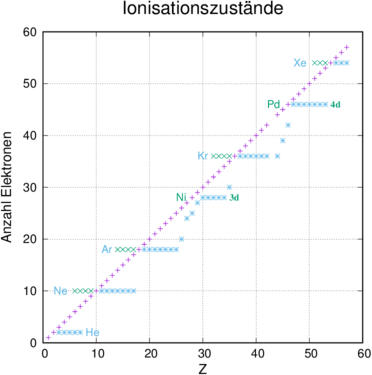
Ionisationszustände nach [HW04, p. 349].
_____________________________________________________________________
Eine Tabelle aller Elektronenkonfigurationen, Ionisationsenergien und Schalen aller Elemente finden Sie im Anhang B.