Weiter: Aggregatszustände Oben: Wärmelehre Zurück: Anwendung auf das van-der-Waals-Gas Skript: PDF-Datei Übungen: Blätter
![\includegraphics[width=0.5\textwidth]{thermodynamik-007}](img2314.gif)
|
Beim Überströmversuch nach Abbildung 4.55 mit einem idealen Gas bleibt die Temperatur erhalten,
da
![]() ist. Erst wenn wir den Versuch mit einem realen Gas durchführen, erhalten wir eine
Temperaturänderung.
ist. Erst wenn wir den Versuch mit einem realen Gas durchführen, erhalten wir eine
Temperaturänderung.
Auch beim realen Gas bleibt die Gesamtenergie (ein abgeschlossenes System) erhalten.
| (4.581) |
Bei einem realen Gas ziehen sich die Moleküle jedoch an. Beim Expandieren entfernen sie sich voneinander. Dadurch wird Energie benötigt, um sie der bei kleinen Distanzen negativeren potentiellen Energie zu höheren Werten zu bewegen. Diese Energie muss von der kinetischen Energie geliefert werden. Die Moleküle bewegen sich langsamer. Damit ist das Gas abgekühlt worden. Die Grösse der Abkühlung ist ein Mass für die Grösse der Anziehungskräfte.
Aus der van-der-Waals-Gleichung (4.297) folgt mit
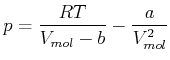 |
Andererseits betrachten wir den ersten Hauptsatz
![]() . Wir teilen durch
. Wir teilen durch ![]() und erhalten
und erhalten
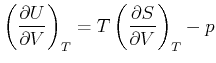 |
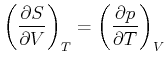 |
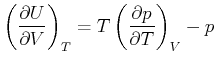 |
(4.583) |
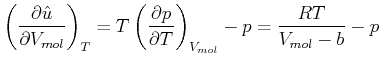 |
(4.584) |
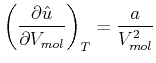 |
(4.585) |
Mit der Gleichung (4.281) bekommen wir
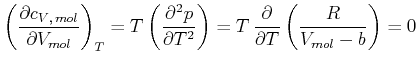 |
(4.586) |
Die molare Wärmekapazität bei konstantem Volumen hängt also nicht vom Volumen ab, sondern nur von der Temperatur
| (4.587) |
Damit kann dass Differential der molaren inneren Energie wie folgt geschrieben werden:
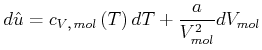 |
(4.588) |
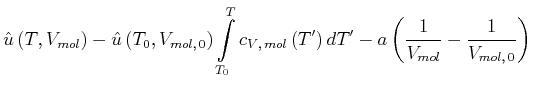 |
(4.589) |
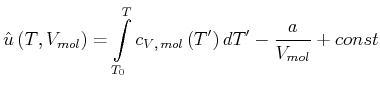 |
(4.590) |
Betrachten wir einen Prozess mit einer kleinen Temperaturänderung
![]() , so ist die molare
Wärmekapazität bei konstantem Volumen konstant.
, so ist die molare
Wärmekapazität bei konstantem Volumen konstant.
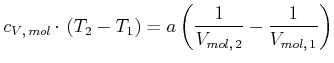 |
(4.592) |
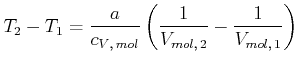 |
(4.593) |
|
Der Überströmversuch sagt aus, wie gut ein Gas das ideale Gas
approximiert. Aus der Temperaturerniedrigung kann der Binnendruck |
![\includegraphics[width=0.5\textwidth]{thermodynamik-008}](img2343.gif)
|
Beim Überströmversuch wie im vorherigen Abschnitt beschrieben ist das Gas nicht im Gleichgewicht. Deshalb modifizieren wir den Überströmkanal wie in Abbildung 4.56 gezeigt. Eine poröse Masse, ein Wattestopfen beispielsweise, ermöglicht, dass das Gas während dem gesamten Expansionsprozess im Gleichgewicht ist. Das Gas leistet Arbeit an dem Stopfen.
![\includegraphics[width=0.95\textwidth]{thermodynamik-009}](img2344.gif)
|
Abbildung 4.57 wird verwendet, um die Thermodynamik des Ausströmens im Gleichgewicht zu berechnen. Die Änderung der Energie ist
Die mechanische Arbeit ist
| (4.595) |
| (4.596) |
|
Beim Überströmversuch mit einem porösen Stopfen bleibt die Enthalpie |
Als Gleichung geschrieben, bedeutet dies
| (4.597) |
Für ein ideales Gas können wir mit der Zustandsgleichung schreiben
| (4.598) |
Das allgemeine Differential der Enthalpie ist
| (4.599) |
| 0 | ![$\displaystyle =dH=T\left[ \left( \frac{\partial S}{\partial T}\right) _{p}dT+\left( \frac{\partial S}{\partial p}\right)_T dp\right] +Vdp$](img2356.gif) |
|
| 0 | ![$\displaystyle =C_{p}dT+\left[ T\left( \frac{\partial S}{\partial p}\right) _{T}+V\right] dp$](img2357.gif) |
(4.600) |
Beim Joule-Thomson-Effekt ist die Enthalpie konstant. Die Änderung der Temperatur mit dem Druck ist dann gegeben durch
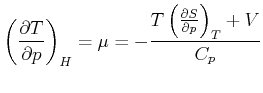 |
(4.601) |
![]() ist der Joule-Thomson-Koeffizient. Seine Einheit ist
ist der Joule-Thomson-Koeffizient. Seine Einheit ist
![$\displaystyle \left[\mu\right] = \frac{K}{Pa} = \frac{m^2 K}{N}$](img2360.gif) |
Mit der Definition des Volumenausdehnungskoeffizienten und einer Maxwellrelation erhalten wir
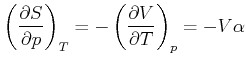 |
(4.602) |
Für ideale Gase gilt
![]() .
.
|
Für ideale Gase ist der Joule-Thomson-Koeffizient
|
Bei realen Gasen kann ![]() sowohl positiv wie negativ sein.
sowohl positiv wie negativ sein.
Die Kurve
![]() heisst Inversionskurve.
heisst Inversionskurve.
![\includegraphics[width=0.5\textwidth]{thermodynamik-010}](img2371.gif)
Kurven konstanter Enthalpie
|
Die maximale Temperatur, bei der ![]() ist, heisst Inversionstemperatur
ist, heisst Inversionstemperatur ![]() .
.
|
|
Die molare Enthalpie ![]() von van-der-Waals-Gasen ist
von van-der-Waals-Gasen ist
Da die Enthalpie konstant ist, berechnen wir
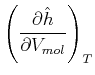 |
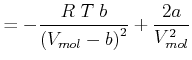 |
(4.606) |
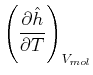 |
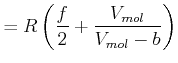 |
(4.607) |
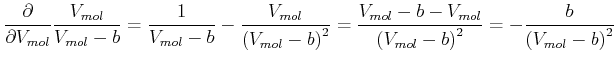 |
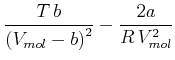 |
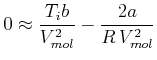 |
Damit wird die Inversionstemperatur
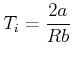 |
(4.609) |
Wir hatten für das van-der-Waals-Gas die kritische Temperatur
![]() ausgerechnet. Sie hing, wie
die Inversionstemperatur
ausgerechnet. Sie hing, wie
die Inversionstemperatur ![]() nur von
nur von ![]() und
und ![]() ab. Also sind
ab. Also sind ![]() und
und ![]() voneinander abhängig.
voneinander abhängig.
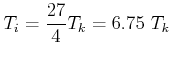 |
(4.610) |
![\includegraphics[width=0.7\textwidth]{thermodynamik-011}](img2400.gif)
|
Gase werden in der Regel mit dem Linde-Verfahren verflüssigt (siehe Abbildung 4.59). Beim
Linde-Verfahren wird Gas durch einen Kompressor durch eine poröse Ausströmdüse gedrückt. ist die
Anfangstemperatur unter der Inversionstemperatur ![]() , wird das Gas bei der Expansion abgekühlt. Um den Prozess
effizienter zu machen, wird das einströmende Gas durch einen Gegenstromkühler vorgekühlt. Ist das Gas genügend
vorgekühlt, wird bei der Expansion die Temperatur so stark abgesenkt, dass das Gas verflüssigt wird. Stickstoff
(
, wird das Gas bei der Expansion abgekühlt. Um den Prozess
effizienter zu machen, wird das einströmende Gas durch einen Gegenstromkühler vorgekühlt. Ist das Gas genügend
vorgekühlt, wird bei der Expansion die Temperatur so stark abgesenkt, dass das Gas verflüssigt wird. Stickstoff
(![]() ) hat eine Inversionstemperatur von
) hat eine Inversionstemperatur von ![]() und kann also mit dem Linde-verfahren direkt ohne weitere
Hilfsmittel verflüssigt werden. Wasserstoff (
und kann also mit dem Linde-verfahren direkt ohne weitere
Hilfsmittel verflüssigt werden. Wasserstoff (![]() hat eine Inversionstemperatur, die unterhalb der Raumtemperatur
liegt. Wasserstoff muss zum Beispiel mit flüssiger Luft vorgekühlt werden.
hat eine Inversionstemperatur, die unterhalb der Raumtemperatur
liegt. Wasserstoff muss zum Beispiel mit flüssiger Luft vorgekühlt werden.
Helium mit einer Inversionstemperatur von ![]() müsste mit
müsste mit ![]() vorgekühlt werden, damit es im Linde-Verfahren
durch den Joule-Thomson-Effekt verflüssigt werden kann. Dieses Verfahren wird nicht verwendet, da es zwar
physikalisch möglich, aber viel zu gefährlich ist. Wie verflüssigt man also
vorgekühlt werden, damit es im Linde-Verfahren
durch den Joule-Thomson-Effekt verflüssigt werden kann. Dieses Verfahren wird nicht verwendet, da es zwar
physikalisch möglich, aber viel zu gefährlich ist. Wie verflüssigt man also ![]() ? man entzieht dem
? man entzieht dem ![]() innere
Energie, indem man es in einer Turbine Arbeit leisten lässt!
innere
Energie, indem man es in einer Turbine Arbeit leisten lässt!
Wir haben bis jetzt die Zustandsgleichung des idealen Gases
| (4.612) |
Wir können die Virialkoeffizienten des van-der-Waals-Gases bestimmen, indem wir Gleichung (4.339) in eine Potenzreihe (Taylorreihe) entwickeln.
|
Der Virialkoeffizient ![]() des van-der-Waals-Gases hängt von der Temperatur ab, die höheren
Virialkoeffizienten nicht. Beim idealen gas sind alle Virialkoeffizienten identisch null.
des van-der-Waals-Gases hängt von der Temperatur ab, die höheren
Virialkoeffizienten nicht. Beim idealen gas sind alle Virialkoeffizienten identisch null.
| Dieser Stoff wurde am 12. 07. 2007 behandelt |
|
|
Materialien
Folien zur Vorlesung am 12. 07. 2007 PDF |
Wir erhalten die erste Näherung der Zustandsfunktion eines realen Gases, wenn wir nur den Virialkoeffizienten
![]() berücksichtigen.
berücksichtigen.
| (4.615) |
| (4.616) |
![\includegraphics[width=0.5\textwidth]{thermodynamik-012}](img2418.gif)
Temperaturverlauf des Virialkoeffizienten
|
Wenn, was die Regel ist,
![]() kann
kann
![]() durch
durch
![]() ersetzt werden
(Annahme des idealen Gases). Wir erhalten
ersetzt werden
(Annahme des idealen Gases). Wir erhalten
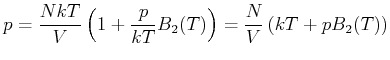 |
(4.617) |
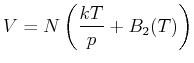 |
(4.618) |
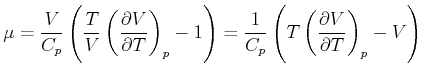 |
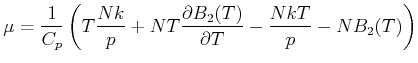 |
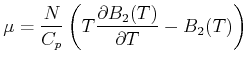 |
(4.619) |
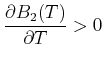 |
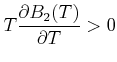 |
Othmar Marti